
题目列表(包括答案和解析)
A.SO2、O2分别为0.4 mol·L-1、0.2 mol·L-1
B.SO2为0.20 mol·L-1
C.SO2、SO3均为0.15 mol·L-1
D.SO2为0.24 mol·L-1,SO3为0.16 mol·L-1
将两种浓度都是1 mol·L-1的气体X2、Y2在密闭容器中反应生成Z,某时刻测得各物质的浓度分别是c(X2)=0.58 mol·L-1,c(Y2)=0.16 mol·L-1,c(Z)=0.84 mol·L-1,则Z的化学式为( )
A.XY B.XY2 C.X2Y D.XY3
A.XY B.XY2 C.X2Y D.XY3
(共16分,没空2分)
已知下列热化学方程式:
①C(s)+H2O(s)===CO(g)+H2(g) ΔH=-131.3 kJ·mol-1
②H2SO4(l)+NaOH(l)===Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1
③C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+O2(g)===CO2(g) ΔH=-283 kJ·mol-1
⑤HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑥H2(g)+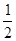 O2(g)===H2O(1) ΔH=-285.6kJ/mol
O2(g)===H2O(1) ΔH=-285.6kJ/mol
⑦C3H8(g)+5O2(g) ===3CO2(g)+4H2O(1) ΔH=-2220.0 kJ·mol-1
⑧ N2 (g)+ 3H2(g)="==" 2NH3 (g) ΔH=-92 kJ·mol-1
(1)上述热化学方程式中,不正确的有______________,不正确的理由分别是 _____________________________________________________________________________。
(2)根据上述信息,写出C转化为CO的热化学方程式:______________________。
(3)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热6262.5kJ,则混合气体中H2和C3H8的体积比是 。
(4)已知:H2O(1)=H2O(g);ΔH=+44.0kJ/mol写出丙烷燃烧生成CO2和气态水的热化学方程式
(5)上述反应中,表示燃烧热的热化学方程式有__________________________________;
表示中和热的热化学方程式有______________。
(6) 已知H—H键能为436 kJ/mol,H—N键能为391kJ/mol,则N≡N键的键能是_____________?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com