
题目列表(包括答案和解析)
CuSO4∙5H2O是铜的重要化合物,有着广泛的应用。CuSO4∙5H2O的实验室制法如下:
Ⅰ.实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程(Fe3+在pH=5时已完全沉淀)

回答下列问题:
⑴用98%的浓硫酸配制溶解所用的4.5 mol∙L-1的稀硫酸,只需 种玻璃仪器
⑵步骤②目的是将溶液Ⅰ中的Fe2+充分转化成Fe3+,实验操作是
发生反应的离子方程式:
⑶如何证明Fe2+已经充分转化?
⑷步骤④之后的实验操作是 ,所需仪器是铁架台(带铁圈)、
及抽滤装置。
Ⅱ.实验室用铜粉制备的CuSO4∙5H2O流程图如下:
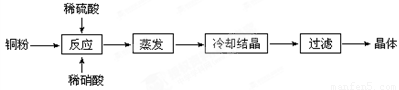
根据题意完成下列填空:
⑴理论上,为了制得纯净的CuSO4·5H2O晶体,需要消耗稀硫酸、稀硝酸溶质物质的量之比为 ,
发生反应的离子方程式为 。
⑵实际制得的胆矾晶体中还是含有一些杂质,通常采用 法提纯。
⑶实际生产过程中对所加稀硝酸的浓度控制要求比较高,通常用标准氢氧化钠溶液来滴定。滴定过程中若用酚酞作指示剂,终点现象是
。
请在图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。

⑷上述使用的标准氢氧化钠溶液已经通过基准物质的标定。下列物质中通常可用来标定碱液的基准物质是 。
A.醋酸 B.草酸 C.苯甲酸 D.苯酚

CuSO4?5H2O是铜的重要化合物,有着广泛的应用。CuSO4?5H2O的实验室制法如下:
Ⅰ.实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程(Fe3+在pH=5时已完全沉淀)
回答下列问题:
⑴用98%的浓硫酸配制溶解所用的4.5 mol?L-1的稀硫酸,只需 种玻璃仪器
⑵步骤②目的是将溶液Ⅰ中的Fe2+充分转化成Fe3+,实验操作是
发生反应的离子方程式:
⑶如何证明Fe2+已经充分转化?
⑷步骤④之后的实验操作是 ,所需仪器是铁架台(带铁圈)、
及抽滤装置。
Ⅱ.实验室用铜粉制备的CuSO4?5H2O流程图如下:
根据题意完成下列填空:
⑴理论上,为了制得纯净的CuSO4·5H2O晶体,需要消耗稀硫酸、稀硝酸溶质物质的量之比为 ,
发生反应的离子方程式为 。
⑵实际制得的胆矾晶体中还是含有一些杂质,通常采用 法提纯。
⑶实际生产过程中对所加稀硝酸的浓度控制要求比较高,通常用标准氢氧化钠溶液来滴定。滴定过程中若用酚酞作指示剂,终点现象是
。
请在图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。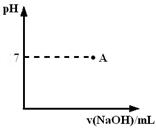
⑷上述使用的标准氢氧化钠溶液已经通过基准物质的标定。下列物质中通常可用来标定碱液的基准物质是 。
| A.醋酸 | B.草酸 | C.苯甲酸 | D.苯酚 |
CuSO4·5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。
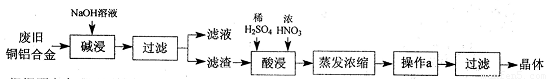
根据题意完成下列填空:
(1)“碱浸”的目的是 ,写出有关的离子方程式 。
(2)向滤渣中先加入足量稀硫酸,然后再滴加少量浓硝酸,在废渣溶解时可以观察到的实验现象有 。
(3)操作a的名称为 ,制得的CuSO4·5H2O中可能存在硝酸铜杂质,除去这种杂质的实验操作名称为 。
(4)已知:CuSO4+2NaOH=Cu(OH)2↓+ Na2SO4。称取0.26 g提纯后的CuSO4·5H2O试样于锥形瓶中,加入0.1000 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸8.00 mL,则该试样中CuSO4·5H2O的质量分数为 ;上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用 。
(5)在“酸浸”的步骤中,①若只加入浓硫酸,写出加热时的化学方程式 。
②若将浓硝酸换成过氧化氢,常温时即可生成硫酸铜,指出此种方法的优点 。
(12分)CuSO4·5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。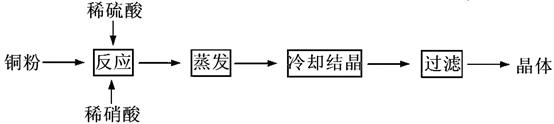
根据题意完成下列填空:
(1)理论上,为了制得纯净的CuSO4·5H2O晶体,需要消耗稀硫酸、稀硝酸溶质物质的量之比为 ,发生反应的离子方程式为 。
(2)实际制得的胆矾晶体中还是含有一些杂质,通常采用 法提纯。
(3)实际生产过程中对所加稀硝酸的浓度控制要求比较高,通常用标准氢氧化钠溶液来滴定。滴定过程中若用酚酞作指示剂,终点现象是 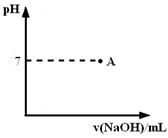 。请在右图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。
。请在右图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。
(4)上述使用的标准氢氧化钠溶液已经通过基准物质的标定。下列物质中通常可用来标定碱液的基准物质是 。
| A.醋酸 | B.草酸 | C.苯甲酸 | D.苯酚 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com