
题目列表(包括答案和解析)
(17分)
镇痉药物C、化合物N以及高分子树脂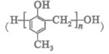 的合成路线如下:
的合成路线如下: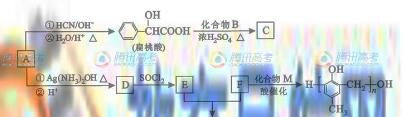
已知:
(1)A的含氧官能团的名称是________。
(2)A在催化剂作用下可与H2 反映生成B。该反应的反应类型是_________。
(3)酯类化合物C的分子式是C15H14O3 ,其结构简式是_______。
(4)A发生银镜反应的化学方程式是_________。
(5)扁桃酸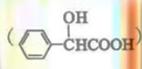 由多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有 种,写出其中一种含亚甲基
由多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有 种,写出其中一种含亚甲基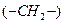 的同分异构体的结构简式__________。
的同分异构体的结构简式__________。
(6)F与M合成高分子树脂的化学方程式是___________。
(7)N在NaOH溶液中发生水解反应的化学方程式是_____________。
(17分)卡托普利OE)是用于治疗各种原发性高血压的常用药物,可由下列路线合成:
(1) A的结构简式是_______, B中含有官能团的名称是_______。
(2) C→D的反应类型是_______
(3) 已知: (高分子化合物),则
(高分子化合物),则
B→F的化学方程式为____________________________;
高分子化合物H的结构简式为_____________________。
(4) D的消去产物 有多种同分异构体,如
有多种同分异构体,如 等。写出其中满足下列条件的同分异构体:
等。写出其中满足下列条件的同分异构体:
(i) 含有苯环,不含甲基
(ii) 能与NaOH溶液以物质的量之比1:1完全中和
(iii) 苯环上一卤代物只有一种
___________________________________、____________________________
(5) 下列关于卡托普利(¾的说法正确的是_______。
a.能发生取代反应 b.在氧气中充分燃烧的产物有SO2
c.能与Na反应生成氢气 d. E的分子式为
(12分)(2011·银川高二检测)化学反应过程中发生物质变化的同时,常常伴有能量的变化,这种能量的变化常以热能的形式表现出来,叫做反应热。由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等。
(1)下列ΔH表示物质燃烧热的是________;表示物质中和热的是________。(填ΔH1、ΔH2和ΔH3等)
A.2H2(g)+O2(g)===2H2O(l) ΔH1
B.C(s)+O2(g)===CO(g) ΔH2
C.CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH3
D.C(s)+O2(g)===CO2(g) ΔH4
E.C6H12O6(s)+6O2(g)===6CO2(g)+6H2O(l) ΔH5
F.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH6
G.2NaOH(aq)+H2SO4(aq)===Na2SO4(aq)+2H2O(l) ΔH7
(2)进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键时所需吸收的能量。下表是部分化学键的键能数据:
|
化学键 |
P—P |
P—O |
O===O |
P===O |
|
键能kJ/mol |
197 |
360 |
499 |
x |
已知白磷(P4)的燃烧热为2 378.0 kJ/mol,白磷完全燃烧的产物(P4O10)的结构如图所示,则上表中x=________。

(8分)(2011·泰州模拟)某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 实验 序号 | 时间 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(17分,每空1分,特别说明的除外)下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ______,⑥ ______,⑦ __ __。
(2)画出原子的结构示意图:④___ __ ___,⑧___ 。
(3)在①~12元素中,金属性最强的元素是_____,非金属性最强的元素是______,最不活泼的元素是____。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.常温下⑦的单质和⑧的单质状态不同b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是 (填序号),跟它同周期原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物,用电子式表示其形成过程如下: (2分)。
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com