
题目列表(包括答案和解析)
(12分)
碳、硫的含量影响钢铁性能,碳、硫含量的一种测定方法是将钢样中碳、硫转化为气体,再用测碳、测硫装置进行测定。
(1)采用装置A,在高温下x克钢样中碳、硫转化为CO2、SO2。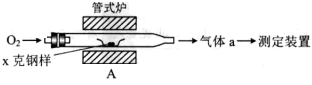
①气体a的成分是____________________。
②若钢样中硫以FeS形式存在,A中反应:3FeS+5 O2高温1____+3_____。
(2)将气体a通入测硫酸装置中(如右图),采用滴定法测定硫的含量。
①H2O2氧化SO2的化学方程式:_________________。
②用NaOH溶液滴定生成的H2SO4,消耗z mLNaOH溶液,若消耗1mLNaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数:_________________。
(3)将气体a通入测碳装置中(如下图),采用重量法测定碳的含量。

①气体a通过B和C的目的是_____________________。
②计算钢样中碳的质量分数,应测量的数据是__________________。



钢铁中碳、硫的含量对钢材的物理性能和机械性能影响很大.某研究性学习小组拟测定钢样中碳的含量.查资料知:SO2可以和石灰水反应,可以被KMnO4溶液氧化,也可以使一种叫品红的溶液褪色(该反应常用来检验SO2).他们设计了如下实验:将钢样充分灼烧,使其中的碳、硫全部转化为CO2、SO2逸出,吸收气体的装置如下:
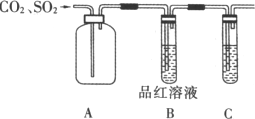
(1)A中应放入________;
(2)B中放入品红溶液的作用是:________;
(3)若KMnO4的还原产物为Mn2+,则KMnO4与SO2反应的物质的量之比为________;
(4)用m g钢样充分灼烧反应,通过过量石灰水吸收,经分离、干燥得沉淀n g,则该钢样中的含碳量为________(用含m、n的代数式表示)
(5)装置中可能对测定含碳量结果产生影响的因素有________(写出任意一种合理的即可).
为了探究浓度对硫酸氧化性的影响,某学习小组进行了以下探究活动:
[探究一]
称取无锈铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
(1)甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中的Fe2+,请选择下列试剂,设计简单的实验方案(简述操作过程、现象和结论) 。
(供选用试剂:.KSCN溶液,氯水,铁粉,.浓氨水 ,酸性KMnO4溶液。)
(2)乙同学为了测定气体Y中SO2的含量,设计如下三种方案:
方案I:取672mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g。
方案II:向VmL c mol·L-1酸性高猛酸钾溶液中缓慢通入Y气体aL(标准状况),溶液恰好完全褪色。
方案III:取VL(标准状况)气体Y缓慢通入足量的氢氧化钡溶液中,充分反应后,过滤、洗涤、烘干,称得固体质量为mg。
其中不合理的方案是 ,理由是 。
[探究二]
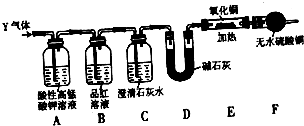
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体。为此设计了下列探究实验装置(图中夹持装置已省略)。
(3)装置A中试剂的作用是 。
(4)简述确认气体Y中含有CO2的实验现象: 。
(5)有同学根据“F干燥管无水硫酸铜是否变蓝色”确认Y气体中是否有氢气,你认为是否可靠? (填“可靠”或“不可靠”),简述理由: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com