
题目列表(包括答案和解析)
下表是元素周期表一部分,列出了十个元素在周期表中的位置:
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | | | | ⑥ | ⑦ | | | |
| 3 | ① | ③ | ⑤ | | | | ⑧ | ⑩ |
| 4 | ② | ④ | | | | | ⑨ | |
下表是元素周期表一部分,列出了十个元素在周期表中的位置:
|
族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
|
|
|
⑥ |
⑦ |
|
|
|
|
3 |
① |
③ |
⑤ |
|
|
|
⑧ |
⑩ |
|
4 |
② |
④ |
|
|
|
|
⑨ |
|
请用化学用语回答下列问题
(1)在③~⑦元素中,原子半径最大的是 (填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是 (填物质化学式),呈两性的氢氧化物是 (填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有 ;
(4)用电子式表示元素③与⑧形成化合物的过程 。
(5)写出含有32个电子的元素⑥的氢化物的分子式: 。
(6)写出工业冶炼⑤的化学方程式:
(7)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2 第二步: ; 第三步Cl2+2Br-=2Cl-+Br2
下表是元素周期表一部分,列出了十个元素在周期表中的位置:
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
请用化学用语回答下列问题
(1)在③~⑦元素中,原子半径最大的是 (填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是 (填物质化学式),呈两性的氢氧化物是 (填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有 ;
(4)用电子式表示元素③与⑧形成化合物的过程 。
(5)写出含有32个电子的元素⑥的氢化物的分子式: 。
(6)写出工业冶炼⑤的化学方程式:
(7)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2 第二步: ; 第三步Cl2+2Br-=2Cl-+Br2
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | =10 ⑩ | |||




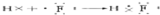
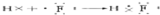
| ||
| ||
| a | |||||||
| b | c | d | |||||
| e | f | g | |||||


| ||
| △ |
| ||
| △ |
| ||
| ||
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com