
题目列表(包括答案和解析)

 2NO2(g)在前1l0s内的反应进
2NO2(g)在前1l0s内的反应进
| [NO2]2 |
| [N2O4] |
| [NO2]2 |
| [N2O4] |

 2NO2(g)在前1l0s内的反应进
2NO2(g)在前1l0s内的反应进

 2NO2(g)在前1l0s内的反应进
2NO2(g)在前1l0s内的反应进
自然界中氮的循环涉及到地球上生物圈的方方面面。人类进入工业化社会以后,化学合成氮肥的数量迅速上升,对氮的循环和环境影响很大。下图是工业合成氮肥的转化关系:
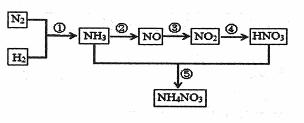
回答下列问题:
(1)反应①的条件是 ,反应④的化学方程式为 ,
反应⑤所得产物的溶液中离子浓度由大到小得顾序为 。
(2)实验室制取NH3的一种方法是在生石灰中滴加浓氨水,其原因是
。
(3)硝酸厂的尾气含有氮的氧化物,直接排放将污染空气。目前科学家探索利用燃料
气体中的CH4等将氮的氧化物还原为N2和H2O,反应原理为:
![]()
![]()
则![]() 直接将NO2还原为N2的热化学方程式为 。 .
直接将NO2还原为N2的热化学方程式为 。 .
(4)下图表示某温度时,反应N2O4(g)![]() 2NO2(g)在前1l0s内的反应进
2NO2(g)在前1l0s内的反应进
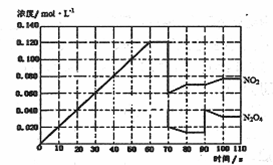
①此反应的平衡常数表达式K= 。
②反应进行到70s时,改变的条件可能是 (填字母) , 反应进行到90s时,改变的条件可能是 (填字母)
A.加入催化剂 B.扩大容器体积 C.升高温度 D.增大N2O4的浓度
③请在图中画出反应物N2O4在0~70秒时的浓度变化曲线。
(8分)
KClO3热分解是实验室制取氧气的一种方法。KClO3在不同的条件下热分解结果如下:
实验 | 反应体系 | 第一放热温度/℃ | 第二放热温度/℃ |
A | KClO3 | 400 | 480 |
B | KClO3+Fe2O3 | 360 | 390 |
C | KClO3+MnO2 | 350 |
|
已知⑴K(s)+1/2Cl2(g)=KCl(s) △H![]() (1)=-437 kJ?mol-1
(1)=-437 kJ?mol-1
⑵K(s)+1/2Cl2+3/2O2(g)= KClO3(s) △H![]() (2)=-398 kJ?mol-1
(2)=-398 kJ?mol-1
⑶K(s)+1/2Cl2+2O2(g)= KClO4(s) △H![]() (3)=-433 kJ?mol-1
(3)=-433 kJ?mol-1
7-1 根据以上数据,写出上述三个体系对应的分解过程的热化学方程式。
7-2 用写MnO2催化KClO3分解制得的氧气有轻微的刺激性气味,推测这种气体是什么,并提出确认这种气体的实验方法。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com