
题目列表(包括答案和解析)
- 4 |
2- 4 |
2- 4 |
1 4 |
2- 4 |
2- 4 |
(16分)
A是面粉中的主要成分,C与E反应可生成F,D能与新制的Cu(OH)2悬浊液反应产生砖红色沉淀。下图是A、B、C、D、E、F等几种常见有机物之间的转化关系图:
根据以上信息完成下列各题:
(1)A的化学式为____________,B的名称为_____________。
(2)C的结构简式为__________,D的结构简式为__________,F的结构简式为__________。
(3)C和E反应生成F的化学方程式为_________________________________。
(4)E与小苏打溶液反应的化学方程式为_______________________________________。
(10分)已知高锰酸钾、二氧化锰在酸性条件下能将草酸钠(Na2C2O4)氧化:
MnO4—+C2O42—+H+―→Mn2++CO2↑+H2O(未配平);
MnO2+C2O42—+H+―→Mn2++CO2↑+H2O(未配平)。
为测定某软锰矿中二氧化锰的质量分数,准确称量1.20 g软锰矿样 品,加入2.68 g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到容量瓶中用蒸馏水稀释至刻度,从中取出25.0 mL,用0.0200 mol·L-1高锰酸钾溶液进行滴定。当加入20.0 mL溶液时恰好完全反应,试根据以上信息完成下列各题:
品,加入2.68 g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到容量瓶中用蒸馏水稀释至刻度,从中取出25.0 mL,用0.0200 mol·L-1高锰酸钾溶液进行滴定。当加入20.0 mL溶液时恰好完全反应,试根据以上信息完成下列各题:
(1)配平上述两个离子方程式:
___MnO+___C2O+___H+===___Mn2++___CO2↑+___H2O;
___MnO2+__C2O+___H+===___Mn 2++___CO2↑+__H2O。
2++___CO2↑+__H2O。
(2)欲求得软锰矿中二氧化锰的质量分数,还缺一个数据,这个数据是__________(填数据所代表的意义)。
(3)若该数据的数值为250,求该软锰矿中二氧化锰的质量分数(写出计算过程)。(4分)
(16分)
A是面粉中的主要成分,C与E反应可生成F,D能与新制的Cu(OH)2悬浊液反应产生砖红色沉淀。下图是A、B、C、D、E、F等几种常见有机物之间的转化关系图:
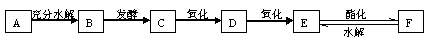
根据以上信息完成下列各题:
(1)A的化学式为____________,B的名称为_____________。
(2)C的结构简式为__________,D的结构简式为__________,F的结构简式为__________。
(3)C和E反应生成F的化学方程式为_________________________________。
(4)E与小苏打溶液反应的化学方程式为_______________________________________。
A~E是原子序数依次增大的五种短周期元素,其性质或结构信息如下表所示
| 元素 | A | B | C | D | E |
| 结构或性质信息 | 单质是空气中主要成分之一,其氢化物水溶液呈碱性 | 原子核外有两个未成对电子 | 日常生活中常见的金属,通常用电解法冶炼其单质 | 其简单阴离子带两个单位负电荷 | 单质有毒,常温下为有色气体,常用于自来水消毒 |
请结合表中信息完成下列各题:
(1)C在元素周期表中的位置是 ,
D的简单阴离子的核外电子排布式为 。
(2)下图是A~E的第一电离能和电负性数据,请回答
①图中序列5是元素 (用元素符号回答)
②下列各组元素最有可能形成离子化合物的是 (填编号)
a.A、B b.A、E c.B、C d.C、E
(3)A的常见单质分子中有多个共价键。
①常温下,该单质化学性质很稳定,是因为
②该单质分子中δ键与π键的数目之比为 。
(4)写出C、E形成的化合物与A的氢化物在水溶液中反应的离子方程式
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com