ЃЈ2013?КЃЕэЧјЖўФЃЃЉСђЛЏЧтЃЈH
2SЃЉЪЧвЛжжОпгаГєМІЕАЦјЮЖЕФЮоЩЋЦјЬхЃЌгаОчЖОЃЛДцдкгкЖржжЩњВњЙ§ГЬвдМАздШЛНчжаЃЎдкШЫЬхЕФКмЖрЩњРэЙ§ГЬжавВЦ№зХживЊзїгУЃЎ
зЪСЯЃКЂйH2SПЩШмгкЫЎЃЈдМ1ЃК2ЃЉЃЌЦфЫЎШмвКЮЊЖўдЊШѕЫсЃЎ
ЂкH2SПЩгыаэЖрН№ЪєРызгЗДгІЩњГЩГСЕэЃЎ
ЂлH2SдкПеЦјжаШМЩеЃЌЛ№бцГЪЕРЖЩЋЃЎ |
ЃЈ1ЃЉФГЛЏбЇаЁзщЩшМЦСЫжЦШЁH
2SВЂбщжЄЦфаджЪЕФЪЕбщЃЌШчЯТЭМЫљЪОЃЎAжаЪЧCuSO
4ШмвКЃЌBжаЗХгаЪЊШѓЕФРЖЩЋЪЏШяЪджНЃЌCжаЪЧFeCl
3ШмвКЃЎ
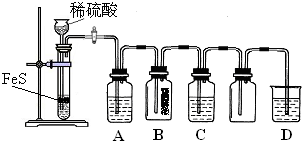
ЛиД№ЯТСаЮЪЬтЃК
ЂйAжагаКкЩЋГСЕэЃЈCuSЃЉВњЩњЃЌAжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ
H2S+CuSO4=CuSЁ§+H2SO4
H2S+CuSO4=CuSЁ§+H2SO4
ЃЎ
ЂкBжаЕФЯжЯѓЪЧ
РЖЩЋЪЏШяЪджНБфКь
РЖЩЋЪЏШяЪджНБфКь
ЃЎ
ЂлCжажЛгаЧГЛЦЩЋГСЕэВњЩњЃЌЧвШмвКБфЧГТЬЩЋЃЎдђCжаЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ
H2S+2Fe3+=SЁ§+2H++2Fe2+
H2S+2Fe3+=SЁ§+2H++2Fe2+
ЃЎ
ЂмDжаЪЂЗХЕФЪдМСПЩвдЪЧ
d
d
ЃЈЬюБъКХЃЉЃЎ
aЃЎЫЎ bЃЎбЮЫс cЃЎNaClШмвК dЃЎNaOHШмвК
ЃЈ2ЃЉЮЊНјвЛВНЬНОП-2МлСђЕФЛЏКЯЮягы+4МлСђЕФЛЏКЯЮяЗДгІЬѕМўЃЌаЁзщЭЌбЇгжЩшМЦСЫЯТСаЪЕбщЃЎ
|
ЪЕбщВйзї |
ЪЕбщЯжЯѓ |
| ЪЕбщ1 |
НЋЕШХЈЖШЕФNa2SКЭNa2SO3ШмвКАДЬхЛ§БШ2ЃК1ЛьКЯ |
ЮоУїЯдЯжЯѓ |
| ЪЕбщ2 |
НЋH2SЭЈШыNa2SO3ШмвКжа |
ЮДМћУїЯдГСЕэЃЌдйМгШыЩйСПЯЁСђЫсЃЌСЂМДВњЩњДѓСПЧГЛЦЩЋГСЕэ |
| ЪЕбщ3 |
НЋSO2ЭЈШыNa2SШмвКжа |
гаЧГЛЦЩЋГСЕэВњЩњ |
вбжЊЃКЕчРыЦНКтГЃЪ§ЃКH
2S K
a1=1.3ЁС10
-7ЃЛK
a2=7.1ЁС10
-15H
2SO
3 K
a1=1.7ЁС10
-2ЃЛK
a2=5.6ЁС10
-8ЂйИљОнЩЯЪіЪЕбщЃЌПЩвдЕУГіНсТлЃКдк
ЫсадЃЈЛђЫсадНЯЧПЃЉ
ЫсадЃЈЛђЫсадНЯЧПЃЉ
ЬѕМўЯТЃЌ+4МлСђЕФЛЏКЯЮяПЩвдбѕЛЏ-2МлСђЕФЛЏКЯЮяЃЎ
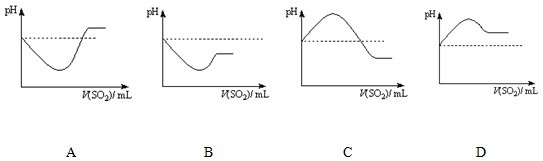
ЂкНЋSO
2ЦјЬхЭЈШыH
2SЫЎШмвКжажБжСЙ§СПЃЌЯТСаБэЪОШмвКpHЫцSO
2ЦјЬхЬхЛ§БфЛЏЙиЯЕЪОвтЭМе§ШЗЕФЪЧ
C
C
ЃЈЬюађКХЃЉЃЎ
ЃЈ3ЃЉЮФЯзМЧдиЃЌГЃЮТЯТH
2SПЩгыAgЗЂЩњжУЛЛЗДгІЩњГЩH
2ЃЎЯжНЋH
2SЦјЬхЭЈЙ§зАгавјЗлЕФВЃСЇЙмЃЌЧыЩшМЦМђЕЅЪЕбщЃЌЭЈЙ§МьбщЗДгІВњЮяжЄУїH
2SгыAgЗЂЩњСЫжУЛЛЗДгІ
НЋЗДгІКѓЕФЦјЬхЭЈШызуСПЧтбѕЛЏФЦШмвКжаЃЈЛђСђЫсЭШмвКЛђТШЛЏЬњШмвКЕШЃЉЃЌГ§ШЅЮДЗДгІЕФH2SКѓЃЌЕуШМЃЌШєЙлВьЕНЛ№бцГЪЕРЖЩЋЃЌЫЕУїгаH2ЩњГЩЃЌДгЖјжЄУїH2SгыAgЗЂЩњСЫжУЛЛЗДгІ
НЋЗДгІКѓЕФЦјЬхЭЈШызуСПЧтбѕЛЏФЦШмвКжаЃЈЛђСђЫсЭШмвКЛђТШЛЏЬњШмвКЕШЃЉЃЌГ§ШЅЮДЗДгІЕФH2SКѓЃЌЕуШМЃЌШєЙлВьЕНЛ№бцГЪЕРЖЩЋЃЌЫЕУїгаH2ЩњГЩЃЌДгЖјжЄУїH2SгыAgЗЂЩњСЫжУЛЛЗДгІ
ЃЎ


