
题目列表(包括答案和解析)
如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡。试回答:
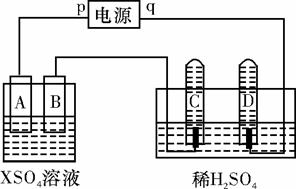
(1)p为 极,A极发生了 反应。
(2)C为 极,试管里收集到的气体是 。
(3)C极的电极反应式是 。
(4)在电解过程中,测得的C、D两极上产生的气体的实验数据如下:
| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极生成气体体积 (cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极生成气体体积 (cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
仔细分析以上实验数据,造成阴、阳两极气体体积比变化的可能原因
是 。
(5)当反应进行一段时间后,A、B电极所在的电解池中溶液的pH (填“增大”、“减小”或“不变”)。
(6)当电路中通过0.004 mol电子时,B电极上沉积金属X为0.128 g,则此金属的摩尔质量为 。
X、Y、Z、W四种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中Y与Z为同一周期,X与W为同一主族,Z元素的外围电子排布为nsnnp2n,W在空气中燃烧可以得到淡黄色固体。又知四种元素分别形成的常见单质在常温常压下有三种是气体,一种是固体。请回答下列问题:
(1)W在元素周期表中的位置是 ;基态时Y的电子排布式是___。
(2)比较元素Y和Z的第一电离能:Y Z(填“大于”、“小于”或“不确定”),将YX3通入溴水中可发生反应,生成Y的单质和一种盐M,Y的单质中的σ键和π键个数比为 ,盐M的晶体类型是 。
(3)由W和Y组成的化合物易水解,其水解的化学方程式是 ;
(4)已知Y2X4和过氧化氢混合可作火箭推进剂。12.8g液态Y2X4与足量过氧化氢反应生成Y的单质和气态水,放出256.65kJ的热量:
2H2O2(l) = O2(g)+2H2O(l) ΔH=-196.4KJ/mol
H2O(l) = H2O(g) ΔH=+44KJ/mol
写出液态Y2X4和氧气反应生成Y的单质和液态X2Z的热化学方程式 。
Ⅰ)⑴已知:N2(g)+O2(g)=2NO(g);△H=+180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905kJ·mol-1
2H2(g)十O2(g)=2H2O(g):△H=-483.6kJ·mol-1
则N2(g)+3H2(g)2NH3(g)的△H= ▲ 。
⑵在一定条件下,将2molN2与5molH2混合于一个10L的密闭容器中,反应情况如图1所示:
①求5min内的平均反应速率v(NH3) ▲ ;
②达到平衡时NH3的体积分数为 ▲ 。
⑶近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图2)。钯电极A上发生的电极反应式是 ▲ 。
Ⅱ)甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
①CH4(g)+H2O(g)CO(g)+3H2(g) ΔH1
②CO(g)+2H2(g)CH3OH(g) ΔH2
将0.20molCH4和0.30molH2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如右图。
(1)温度不变,缩小体积,增大压强,①的反应速率 ▲ (填“增大”、“减小”或“不变”),平衡向 ▲ 方向移动。
(2)反应①的△H1 ▲ 0(填“<”、“=”或“>”)。
Ⅰ)⑴已知:N2(g)+O2(g)=2NO(g);△H=+180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905kJ·mol-1
2H2(g)十O2(g)=2H2O(g):△H=-483.6kJ·mol-1
则N2(g)+3H2(g) 2NH3(g)的△H= ▲ 。
2NH3(g)的△H= ▲ 。
⑵在一定条件下,将2molN2与5molH2混合于一个10L的密闭容器中,反应情况如图1所示:
①求5min内的平均反应速率v(NH3) ▲ ;
②达到平衡时NH3的体积分数为 ▲ 。
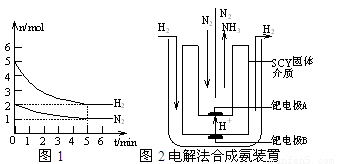
⑶近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图2)。钯电极A上发生的电极反应式是 ▲ 。
Ⅱ)甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
①CH4(g)+H2O(g)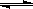 CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1
②CO(g)+2H2(g)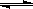 CH3OH(g) ΔH2
CH3OH(g) ΔH2
将0.20molCH4和0.30molH2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如右图。

(1)温度不变,缩小体积,增大压强,①的反应速率 ▲ (填“增大”、“减小”或“不变”),平衡向 ▲ 方向移动。
(2)反应①的△H1 ▲ 0(填“<”、“=”或“>”)。
Ⅰ)⑴已知:N2(g)+O2(g)=2NO(g);△H=+180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H=-905kJ·mol-1
2H2(g)十O2(g)=2H2O(g):△H=-483.6kJ·mol-1
则N2(g)+3H2(g)![]() 2NH3(g)的△H= ▲ 。
2NH3(g)的△H= ▲ 。
⑵在一定条件下,将2molN2与5molH2混合于一个10L的密闭容器中,反应情况如图1所示:
①求5min内的平均反应速率v(NH3) ▲ ;
②达到平衡时NH3的体积分数为 ▲ 。
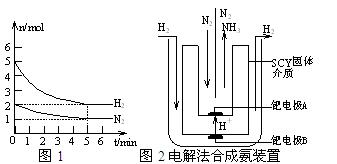
⑶近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图2)。钯电极A上发生的电极反应式是 ▲ 。
Ⅱ)甲醇被称为2l世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。
①CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1
②CO(g)+2H2(g)![]() CH3OH(g) ΔH2
CH3OH(g) ΔH2
将0.20molCH4和0.30molH2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如右图。

(1)温度不变,缩小体积,增大压强,①的反应速率 ▲ (填“增大”、“减小”或“不变”),平衡向 ▲ 方向移动。
(2)反应①的△H1 ▲ 0(填“<”、“=”或“>”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com