
题目列表(包括答案和解析)
 某化学研究小组将锌片和铜片插入某种电解质溶液,锌片和铜片用导线相连,形成原电池装置.
某化学研究小组将锌片和铜片插入某种电解质溶液,锌片和铜片用导线相连,形成原电池装置.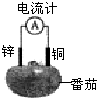 某化学兴趣小组将锌片和铜片出入番茄中制成水果电池(如图)下列说法中正确的是( )
某化学兴趣小组将锌片和铜片出入番茄中制成水果电池(如图)下列说法中正确的是( )某化学研究小组将锌片和铜片插入某种电解质溶液,锌片和铜片用导线相连,形成原电池装置。

(1)若电解质溶液是稀硫酸,则发生氧化反应的是 极(填“锌”或“铜”,下同),溶液中的H+ 移向 极,铜极上的电极反应式是 。
(2)若电解质溶液是硫酸铜溶液,铜极上的电极反应式是 , 若反应过程中有0.2mol电子发生转移,则电解质溶液质量增加 g。
某化学研究小组将锌片和铜片插入某种电解质溶液,锌片和铜片用导线相连,形成原电池装置。
(1)若电解质溶液是稀硫酸,则发生氧化反应的是 极(填“锌”或“铜”,下同),溶液中的H+ 移向 极,铜极上的电极反应式是 。
(2)若电解质溶液是硫酸铜溶液,铜极上的电极反应式是 ,若反应过程中有0.2mol电子发生转移,则电解质溶液质量增加 g。
某化学兴趣小组将锌片和铜片出入番茄中制成水果电池(如右下图)下列说法中正确的是( )
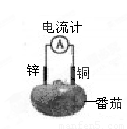
A.一段时间后,锌片质量会变小 B.铜片上发生氧化反应
C.电子由铜片通过导线流向锌 D.锌电极是该电池的正极
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com