
题目列表(包括答案和解析)
根据反应:mA(g) + nB(g) pC(g)
△H ,结合图中所给的信息填空。
pC(g)
△H ,结合图中所给的信息填空。
(填“>”、“=”或“<”)

 ______
______
 ______
______
 ______
______
根据反应:mA(g) + nB(g)![]() pC(g) △H ,结合图中所给的信息填空。
pC(g) △H ,结合图中所给的信息填空。
(填“>”、“=”或“<”)

![]() ______
______![]()
![]() ______
______![]()
![]() ______
______![]()
(6分)利用盖斯定律解答下列各小题
(1)已知反应:H2(g)+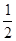 O2(g)==H2O(g) △H1 N2(g)+2O2==2NO2(g) △H2
O2(g)==H2O(g) △H1 N2(g)+2O2==2NO2(g) △H2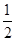 N2(g)+
N2(g)+ H2(g)==NH3(g) △H3
H2(g)==NH3(g) △H3
利用上述三个反应,计算4NH3(g)+7O2(g)==4NO2(g)+6H2O(g)的反应焓变为 (用含△H1、△H2、△H3的式子表示)。
(2) 已知:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+247.4 kJ·mol-1
则以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为: 。
(6分)利用盖斯定律解答下列各小题
(1)已知反应:H2(g)+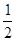 O2(g)==H2O(g)
△H1
N2(g)+2O2==2NO2(g) △H2
O2(g)==H2O(g)
△H1
N2(g)+2O2==2NO2(g) △H2
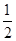 N2(g)+
N2(g)+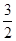 H2(g)==NH3(g)
△H3
H2(g)==NH3(g)
△H3
利用上述三个反应,计算4NH3(g)+7O2(g)==4NO2(g)+6H2O(g)的反应焓变为 (用含△H1、△H2、△H3的式子表示)。
(2) 已知:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+247.4 kJ·mol-1
则以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为: 。
在一定条件下,在1 L密闭容器中发生反应3A(g)+B(g) 2C(g),开始时加入4 mol A、6 mol B,在2 min末时测得C的物质的量是2 mol。
2C(g),开始时加入4 mol A、6 mol B,在2 min末时测得C的物质的量是2 mol。
(1)用A的浓度变化表示反应的平均速率为v(A)=___________;
(2)2 min末时,B的浓度为c(B)=__________;
【解析】考查有关化学反应速率的计算。在有关反应速率的计算时一般采用三段式进行计算,即根据反应式分别列出起始量、转化量和平衡量(或某时刻的量),然后在根据已知条件进行列式计算。即:
3A(g) + B(g) 2C(g)
2C(g)
起始量(mol) 4 6 0
转化量(mol) 3 1 2
2min(mol) 1 5 2
因为反应速率通常用单位时间内浓度的变化量来表示
所以用A的浓度变化表示反应的平均速率为
2 min末时,B的浓度为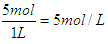
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com