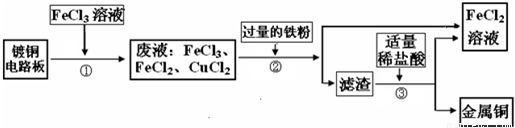
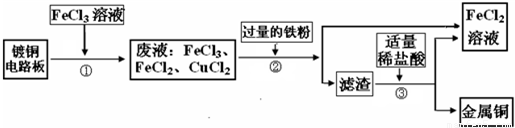
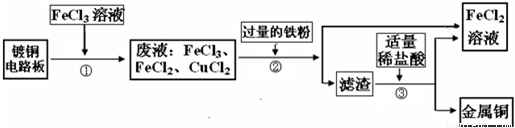
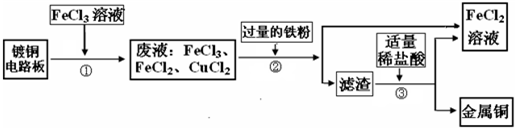
工业上生产电路板及处理废液的工艺流程如下:
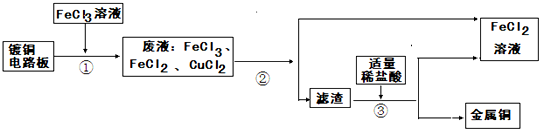
(1)由步骤①可判断与铜反应生成的两种物质是
FeCl2
FeCl2
和
CuCl2
CuCl2
.
(2)步骤②加入过量的铁粉,除能与废液中CuCl
2反应外,还可与FeCl
3发生反应的化学方程式为
Fe+2FeCl3 =3FeCl2
Fe+2FeCl3 =3FeCl2
,该反应属于
化合
化合
反应.
(3)步骤③使用的稀盐酸,是用1体积浓盐酸与5体积的水配制的,在取用浓盐酸时会闻到刺激性气味,用微粒观点解释是
分子在不断地运动
分子在不断地运动
;往滤渣中加入稀盐酸,充分搅拌,当观察到
滤渣中不再有气泡产生
滤渣中不再有气泡产生
现象时,说明滤渣只剩铜.