
题目列表(包括答案和解析)
某实验小组对实验室制取氢气的反应原理进行探究。
【知识回顾】能产生氢气的化学反应有: ①水电解 ②活泼金属与酸反应
【讨论交流】反应①的化学方程式 ;同学们讨论后认为该反应不适用于实验室制取氢气。
【实验探究】为了探究哪种物质更适合用于实验室制取氢气,大家设计了如下实验: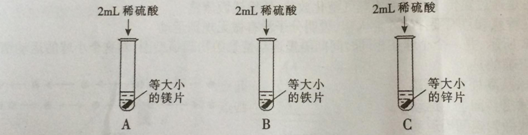
【分析与结论】填写实验报告。
| 实验 | 实验现象 | 实验结论 |
| A | 剧烈反应,迅速产生大量气泡,试管外壁 | 反应速率过快,气体不便收集,不能用于实验室制取氢气 |
| B | 缓慢产生少量气泡 | 反应速率过慢,不能用于实验室制取氢气 |
| C | 较快产生大量气泡,试管外壁发热 | |

| 实验 | 实验现象 | 实验结论 |
| A | 剧烈反应,迅速产生大量气泡,试管外壁 | 反应速率过快,气体不便收集,不能用于实验室制取氢气 |
| B | 缓慢产生少量气泡 | 反应速率过慢,不能用于实验室制取氢气 |
| C | 较快产生大量气泡,试管外壁发热 | |
| ||
| ||


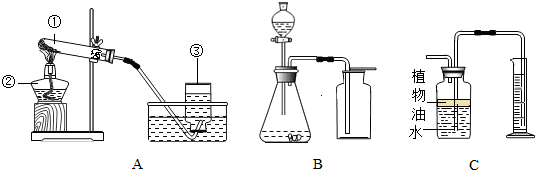
浓度 时间(min) 条件 | 30%H2O2溶液 | 15%H2O2溶液 | 5%H2O2溶液 |
| a克MnO2 | 0.2 | 0.8 | 2.0 |
| a克Fe2O3 | 7.0 | 9.0 | 16.0 |
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | ______ | 木条不复燃 | 常温下过氧化氢溶液不分解 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | ______ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com