ЃЈ2012?еђНЃЉЙЄвЕЬњКьЕФжївЊГЩЗжЪЧFe
2O
3ЃЌЛЙКЌгаЩйСПЕФFeOЁЂFe
3O
4ЃЎЮЊСЫВтЖЈЬњКьжаЬњЕФжЪСПЗжЪ§ЃЌаЫШЄаЁзщЕФЭЌбЇНјааСЫШчЯТЕФЪЕбщЃЌЧыФуВЮгыЙ§ГЬЗжЮіЃЎ
ЁОзЪСЯ1ЁПВнЫсОЇЬхЃЈH
2C
2O
4?3H
2OЃЉдкХЈСђЫсзїгУЯТЪмШШЗжНтЃЌЛЏбЇЗНГЬЪНЮЊЃК
H
2C
2O
4?3H
2O
CO
2Ёќ+COЁќ+4H
2O
ЃЈ1ЃЉЯТСаПЩгУзїВнЫсЗжНтжЦШЁЦјЬхЕФзАжУЪЧ
d
d
ЃЈЬюзжФИБрКХЃЉ
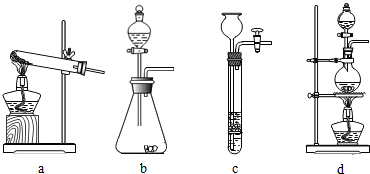
ЁОЮЪЬтЬжТлЁПгУЯТЭМЫљЪОзАжУНјааЪЕбщЃК
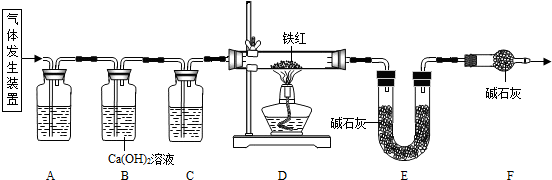
ЃЈ2ЃЉЪЕбщЧАгІЯШ
МьВщзАжУЕФЦјУмад
МьВщзАжУЕФЦјУмад
ЃЎ
ЃЈ3ЃЉНјШыDжаЕФЦјЬхЪЧДПОЛЁЂИЩдяЕФCOЃЌдђAЁЂCжаЕФЪдМСвРДЮЪЧ
c
c
ЁЂ
a
a
ЃЈЬюзжФИБрКХЃЉ
aЃЎХЈСђЫс bЃЎГЮЧхЪЏЛвЫЎ cЃЎЧтбѕЛЏФЦШмвК
ЃЈ4ЃЉBзАжУЕФзїгУЪЧ
бщжЄЖўбѕЛЏЬМвбГ§ОЁ
бщжЄЖўбѕЛЏЬМвбГ§ОЁ
ЃЎ
ЃЈ5ЃЉЖдDзАжУМгШШЧАКЭЭЃжЙМгШШКѓЃЌЖМвЊЭЈШыЙ§СПЕФCOЃЌЦфзїгУЗжБ№ЪЧЃКЂйМгШШЧА
НЋзАжУжаЕФПеЦјХХГіЃЌЗРжЙЗЂЩњБЌеЈ
НЋзАжУжаЕФПеЦјХХГіЃЌЗРжЙЗЂЩњБЌеЈ
ЃЎЭЃжЙМгШШКѓ
Ч§ИЯзАжУжажЭСєЕФЖўбѕЛЏЬМЃЌЪЙЦфШЋВПБЛEзАжУжаМюЪЏЛвШЋВПЮќЪе
Ч§ИЯзАжУжажЭСєЕФЖўбѕЛЏЬМЃЌЪЙЦфШЋВПБЛEзАжУжаМюЪЏЛвШЋВПЮќЪе
ЃЎ
ЃЈ6ЃЉаДГіDзАжУжаЫљЗЂЩњЗДгІЕФвЛИіЛЏбЇЗНГЬЪН
ЃЎ
ЁОЪ§ОнЗжЮігыМЦЫуЁП
ЁОзЪСЯ2ЁПЬњЕФГЃМћбѕЛЏЮяжаЬњЕФжЪСПЗжЪ§ЃК
| ЬњЕФбѕЛЏЮя |
FeO |
Fe2O3 |
Fe3O4 |
| ЬњЕФжЪСПЗжЪ§ |
77.8% |
70.0% |
72.4% |
ЃЈ7ЃЉГЦШЁЬњКьбљЦЗ10.0gЃЌгУЩЯЪізАжУНјааЪЕбщЃЌВтЖЈЬњКьжаЬњЕФжЪСПЗжЪ§ЃЎ
ЂйDжаГфЗжЗДгІКѓЕУЕНFeЗлЕФжЪСПЮЊmgЃЌдђ
7.0
7.0
ЃМmЃМ
7.78
7.78
ЃЎ
ЂкЪЕбщЧАКѓГЦЕУEзАжУдіжи6.6gЃЌдђДЫЬњКьжаЬњЕФжЪСПЗжЪ§ЪЧ
76.0%
76.0%
ЃЎ
ЁОЪЕбщЗДЫМЁП
ЗДЫМ1ЃКБОЪЕбщжаШчЙћШБЩйCзАжУЃЈВЛПМТЧЦфЫќвђЫиЃЉЃЌдђВтЕУбљЦЗжаЬњЕФжЪСПЗжЪ§Лс
ЦЋаЁ
ЦЋаЁ
ЃЈЬюЁАЦЋаЁЁБЁЂЁАВЛБфЁБЛђЁАЦЋДѓЁБЃЉЃЎ
ЗДЫМ2ЃКЧыжИГіЁОЮЪЬтЬжТлЁПжаЪЕбщзАжУЕФвЛИіУїЯдШБЯн
ШБЩйЮВЦјДІРэзАжУ
ШБЩйЮВЦјДІРэзАжУ
ЃЎ


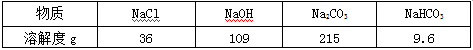

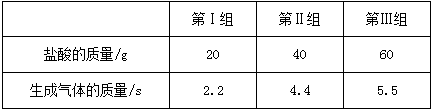
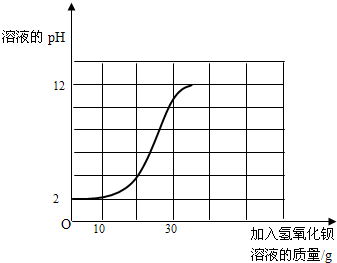 аЁУїЭЌбЇЮЊВтЖЈФГЯЁСђЫсШмвКХЈЖШЃЈМДШмжЪжЪСПЗжЪ§ЃЉЃЌЫћШЁИУЯЁСђЫсШмвК20gЃЌНЋ30gЧтбѕЛЏБЕШмвКЗжШ§ДЮМгШыИУЯЁСђЫсШмвКжаЃЌВтЕУШ§ДЮЗДгІЕФгаЙиЪ§ОнМћЯТБэЃК
аЁУїЭЌбЇЮЊВтЖЈФГЯЁСђЫсШмвКХЈЖШЃЈМДШмжЪжЪСПЗжЪ§ЃЉЃЌЫћШЁИУЯЁСђЫсШмвК20gЃЌНЋ30gЧтбѕЛЏБЕШмвКЗжШ§ДЮМгШыИУЯЁСђЫсШмвКжаЃЌВтЕУШ§ДЮЗДгІЕФгаЙиЪ§ОнМћЯТБэЃК

