
题目列表(包括答案和解析)
Ⅰ.在体积恒定的密闭容器中,充入2mol CO2和5mol H2,一定条件下发生反应: CO2(g) + 3H2(g)  CH3OH(g)
+ H2O(g) △H = -49.0 kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示:
CH3OH(g)
+ H2O(g) △H = -49.0 kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示:

(1)从反应开始到第10min,H2的转化率为 ,在 该条件下,反应的平衡常数K= ,如果在某一时刻保持温度不变,只改变浓度,使c(CO2)=1.00mol/L,c(H2)=0.40mol/L,c(CH3OH)=c(H2O)=0.80mol/L,则平衡 (选填序号)。
a.向正向移动 b.向逆向移动
c.不移动 d.无法确定平衡移动方向
(2)下列措施中能使n(CH3OH)/n(CO2)增大的是 (选填序号)。
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离 d.再充入l mol CH3OH(g)
II.熔融碳酸盐燃料电池(MCFS),发明于1889年。现有一个碳酸盐燃料电池,以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示。请回答下列问题:

(1)A电极的电极反应方程式为 。
(2)常温下,用石墨作电极,以此电源电解一定量的CuSO4 溶液。当两极产生的气体体积相同时停止通电,若电解后溶液的体积为2L,溶液的pH=1(不考虑水解产生的H+),则阳极产生的气体的物质的量是 。
Ⅰ.在体积恒定的密闭容器中,充入2mol CO2和5mol H2,一定条件下发生反应: CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示:
CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示: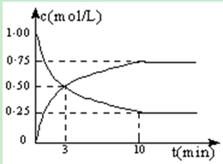
(1)从反应开始到第10min,H2的转化率为 ,在 该条件下,反应的平衡常数K= ,如果在某一时刻保持温度不变,只改变浓度,使c(CO2)=1.00mol/L,c(H2)=0.40mol/L,c(CH3OH)=c(H2O)=0.80mol/L,则平衡 (选填序号)。
a.向正向移动 b.向逆向移动
c.不移动 d.无法确定平衡移动方向
(2)下列措施中能使n(CH3OH)/n(CO2)增大的是 (选填序号)。
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离 d.再充入l mol CH3OH(g)
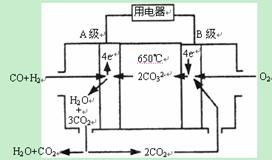
II.熔融碳酸盐燃料电池(MCFS),发明于1889年。现有一个碳酸盐燃料电池,以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示。请回答下列问题:
(1)A电极的电极反应方程式为 。
(2)常温下,用石墨作电极,以此电源电解一定量的CuSO4 溶液。当两极产生的气体体积相同时停止通电,若电解后溶液的体积为2L,溶液的pH=1(不考虑水解产生的H+),则阳极产生的气体的物质的量是 。
 CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示:
CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示: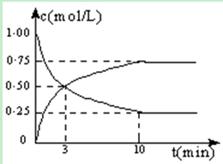
恒温、恒压下,在一个可变容积的密闭容器中发生如下反应:
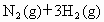
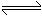
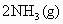
写出该反应的化学平衡常数表达式:K=__________
Ⅰ.若开始时放入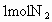 和
和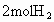 ,到达平衡后,生成
,到达平衡后,生成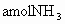 .求:(1)平衡时
.求:(1)平衡时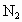 的物质的量为________mol.(用含a的式子表示,以下同)
的物质的量为________mol.(用含a的式子表示,以下同)
(2)原混合气体与平衡混合气体的总物质的量之比,n(始)∶n(平)=________.
(3)达到平衡时,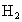 的转化率是_______.
的转化率是_______.
(4)若开始时放入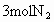 和
和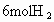 ,到达平衡后,生成
,到达平衡后,生成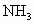 的物质的量为____________mol.
的物质的量为____________mol.
Ⅱ.若维持温度不变,在一个与I反应前起始体积相同、且容积固定的容器中发生上述反应.开始时放入1mol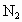 和2mol
和2mol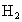 到达平衡后生成bmol
到达平衡后生成bmol .将b与Ⅰ中的a进行比较__________(选填一个编号).
.将b与Ⅰ中的a进行比较__________(选填一个编号).
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
恒温、恒压下,在一个可变容积的密闭容器中发生如下反应:
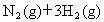
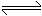
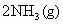
写出该反应的化学平衡常数表达式:K=__________
Ⅰ.若开始时放入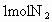 和
和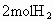 ,到达平衡后,生成
,到达平衡后,生成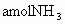 .求:(1)平衡时
.求:(1)平衡时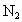 的物质的量为________mol.(用含a的式子表示,以下同)
的物质的量为________mol.(用含a的式子表示,以下同)
(2)原混合气体与平衡混合气体的总物质的量之比,n(始)∶n(平)=________.
(3)达到平衡时,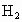 的转化率是_______.
的转化率是_______.
(4)若开始时放入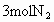 和
和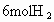 ,到达平衡后,生成
,到达平衡后,生成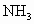 的物质的量为____________mol.
的物质的量为____________mol.
Ⅱ.若维持温度不变,在一个与I反应前起始体积相同、且容积固定的容器中发生上述反应.开始时放入1mol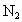 和2mol
和2mol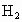 到达平衡后生成bmol
到达平衡后生成bmol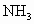 .将b与Ⅰ中的a进行比较__________(选填一个编号).
.将b与Ⅰ中的a进行比较__________(选填一个编号).
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
一、 选择题:(本题包括13小题.共78分)
选择题:(本题包括13小题.共78分)
 (b)
(b) (3分);I2-A2表示数;I1-A1表示数;R2- A2表内阻;R0-定值电阻(1分)
(3分);I2-A2表示数;I1-A1表示数;R2- A2表内阻;R0-定值电阻(1分)
23、(16分)
(1)由图象可知,在0~2s内: (2分)
(2分)
方向沿杆向上 (1分)
在2~4s内: (2分)
(2分)
负号表示方向沿杆向下 (1分)
(2)有风力时的上升过程,由受力分析和牛顿第二定律有:
 ................① (4分)
................① (4分)
 停风后的上升阶段,有:
停风后的上升阶段,有:
A和B达到共同速度v后将不再相对滑动,这段时间为t,有:
 (2分)
(2分)
 (1分)
(1分)
板的最小长度L满足:
 (2分)
(2分)
解得:L=
25、(20分)
(1)从C到A,洛伦兹力不做功,小环对轨道无压力,也就不受轨道的摩擦力.由动能定理,有:
 (3分)
(3分)
 得:s总=
得:s总=
第(3)问评分说明:三种可能性回答任何两种可能性且正确,给满分12分,即每种情况给6分,但第(3)问的总得分不能超过12分.
26.(16分)
(1)Ag+、Ba2+、Al3+ (3分,每答对一个得1分,见错不得分)
(2)(6分,每选择一种正确的离子得1分,每说明一个判断依据正确得2分)
你选择的离子
(每一行填一种离子)
相应的判断依据
CO
溶液中加入过量的盐酸,有气体生成。
AlO
在加入过量盐酸的溶液中,加KHCO3溶液,产生沉淀。
Na+
溶液电中性,至少含有一种阳离子。

(4)3CuO
+ 2NH3  3 Cu + N2 + 3 H2O
3 Cu + N2 + 3 H2O
高温、高压、催化剂(或
高压
28.(14分)
(1)胶头滴管 (1分)
(2)2Fe2+ + Br2 = 2Fe3+ + 2Br― (2分)
(3)取少量最后一次洗出液,滴加AgNO3(或BaCl2)溶液,若无沉淀生成,则证明洗涤干净(合理的答案均可得分) (3分)
(4)再次加热、冷却并称量,直至两次质量差小于
(5)不需要 (1分)
(6)酸式 (1分)
(7)15.90 (2分) 76.00% (或76%)(2分)
29.(16分)

30.(22分)
Ⅰ、10分
(1)①(2分) (2)磷脂(2分) (3)⑦③(2分)
(4)O2+[H] H2O+能量 (2分) (5)④ (2分)
H2O+能量 (2分) (5)④ (2分)
Ⅱ、12分
B组:结果:侧芽生长 (2分)
C组:去掉顶芽,在顶端切口放上含生长素的羊毛脂(3分)
结果:侧芽受抑制不生长 (2分)
D组:用细胞分裂素处理完整植株侧芽 (3分)
结果:侧芽生长 (2分)
31.(20分)
(1)杂交(2分) 纯合子(纯种) (2分)
(2)可以增大种植的密度,增加光合作用面积 (2分)

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com