
题目列表(包括答案和解析)

| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中加KSCN溶液 | 溶液变红色 溶液变红色 |
固体物质中含有FeCl3 |
| 分别向KMnO4溶液中加入适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含 FeCl2 FeCl2 |
| ||
| ||
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,测定溶液pH | pH=0 |
| (2)取少量该溶液加热浓缩,加Cu片和浓 H2SO4,加热 | 有无色气体产生,气体遇空气变成红棕色 |
| (3)取少量该溶液,加少量BaCl2溶液 | 有白色沉淀 |
| (4)取(3)中上层清液,加足量AgNO3溶液 | 有白色沉淀,且不溶于稀HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀,NaOH过量时沉淀部分溶解 |
 Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H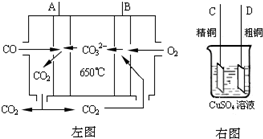
| 10 |
| 11 |
| ||
| 氢离子 |
| 石灰水 |
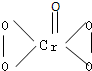
 转化为Cr2O72-.又知:常温时该反应的平衡常数K=1014.上述酸化后所得溶液的pH=______.
转化为Cr2O72-.又知:常温时该反应的平衡常数K=1014.上述酸化后所得溶液的pH=______. Cr3+
Cr3+ Cr(OH)3.用该方法处理10m3 CrO42-的物质的量浓度为1.0×10-3 mol?L-1的废水,至少需要绿矾______Kg(保留两位小数).
Cr(OH)3.用该方法处理10m3 CrO42-的物质的量浓度为1.0×10-3 mol?L-1的废水,至少需要绿矾______Kg(保留两位小数).
 ?
?| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | j | ||||||||||||||||
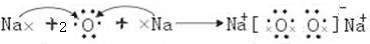
1.A 2.B 3.D 4.A 5.A 6.B 7.B 8.C 9.D 10.C 11.A 12.C
13.(第一空2分,其余空各1分,共6分)
反应物原子间有电子转移 得 降低 还原 还原
14.(空各2分,共6分)②⑦ ①⑧ ④⑤
15.(方程式各3分,共6分)
(1)CaCO3 + 2H+ = Ca2++ 2H2O + CO2↑
(2)Cu2++ SO42- + Ba2++ 2OH-== Cu(OH)2↓+ BaSO4↓
16.(方程式各3分,共6分)
(1)Na2CO3 + 2HC1 = CO2↑+ H2O + 2NaC1
(2)AgNO3+ HC1 = AgC1↓+ HNO3
17.(每小题各2分,共8分) 略。
18.(空各2分,方程式各3分,共14分)
(1)Na2CO3、BaCl2、AgNO3、HCl
(2)CO32- + 2H+ = CO2↑+ H2O ; Ag+ + C1- = AgC1↓
19.(空各3分,共6分) 7.1 7.3
第二章 参考答案
1.B 2.A 3. B 4. C 5. C 6. D 7. C 8. D 9. C 10.B 11.A 12. A
13.银白; Na2O2; 黄; 软;2Na+2H2O=2NaOH+H2↑;(略);Fe3++3OH-=Fe(OH)3↓;
产生红褐色沉淀。
14.风化; 潮解; Na2CO3; 不变。
15.Na+>K+>Rb+; 还原; Rb、K、Na。
16.HCO3-+H+=H2O+CO2↑; 2OH-+CO2=CO32-+H2O; CO32-+H2O+CO2=2HCO3-
17.(1)ac (2)①FeCl3; 2Fe3++Fe=3Fe2+,防止Fe2+被氧化成Fe3+
②产生白色沉淀,迅速变成灰绿色,最终变为红褐色沉淀;4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(3)Al(OH)3, Al(OH)3+OH-=AlO2-+2H2O或Al(OH)3+3H+=Al3++3H2O。
第三章 参考答案
16.18.4%
17.
第四章 参考答案
1.D 2.C 3.C 4.C 5.B 6.C 7.C
8.B 9.C 10.D 11.B 12.D 13.D 14.A
15.③④②①; ④③①②; ④③①②; ③②④①; ④③②①;
16.(1) E C D A B H G F
(2)MnO2+4HCl
(浓)  MnCl2+Cl ↑+2H2O
MnCl2+Cl ↑+2H2O
(3)①除去Cl3中的HCl气体 ②除去Cl2中混有的水蒸气
(4)Cl2+2OH-=Cl-+ClO-+H2O
17.(1)
第五章 参考答案
1.C 2.C 3.B 4.B 5.C 6.B 7.B 8.C 9.C 10.B
11.互为同位素 1:2:3 1:1:1 1:1:1
12.Na2O K2S MgF2 CaCl2
13.(1)A:氧 B:磷 C:硫 D:氯 E:铝
(2) A离子: C原子:
C原子:
(3) 极性
(4)先有白色沉淀产生并逐渐增多,随NaOH加入又逐渐溶解最终澄清
Al3++3OH-=Al(OH)3↓ Al(OH)3+OH-=AlO2-+2H2O
14.(1)A B
(2) ① Cl2+H2O = H+ + Cl‑ + HClO ② 略 ③ 2K2O2+2CO2=2K2CO3+O2
第六章 参考答案
1.B 2.B 3.D 4.D 5.B 6.A 7.B 8.B 9.C 10.D
11.
(1)氧化 (2)还原 (3)
12.(1)①如图配置

②打开分液漏斗上口的活塞,旋开分液漏斗的旋塞,缓慢滴加。
(2)①溶液褪色 ②溶液褪色 ③有浅黄色沉淀(或溶液变浑浊)
(3)①NaSO3 变质 取待测试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再
滴入BaCl2 ,溶液有白色沉淀生成,则证明该NaSO3 固体变质
②不是浓硫酸 用洁净玻璃棒蘸取待测试样,涂白纸不变黑,则证明该溶液不是浓硫酸
13. (1) O2
(1) O2
(2)C + 2H2SO4 (浓) 2SO2 + CO2↑+ 2H2O
(3)CO + 2H+
+ 2H+ CO2↑+
H2O SO2 + Cl2 + 2H2O
4H + + SO + 2Cl ?
+ 2Cl ?
第七章 参考答案
1.D 2.C 3.D 4.B 5.B 6.C 7.D 8.A 9.C 10.C 11.C
12. (1)a、c、d、e? (2)浓HNO3、水、块状大理石
13. (1)B装置中导气管长进短出
(2)①Cu + 2H2SO4(浓) CuSO4 + SO2↑+ 2H2O
CuSO4 + SO2↑+ 2H2O
②反应过程中H2SO4被不断消耗,生成的水逐渐增多,使浓硫酸逐渐变稀,至一定浓度就不再与铜片反应;
③A、D
14.解:⑴ Cu+2H2SO4(浓) CuSO4
+SO2↑+2H2O ⑵Cu
CuSO4
+SO2↑+2H2O ⑵Cu H2SO4
H2SO4  CuSO4
CuSO4
6
⑶c(CuSO4)======0.2mol?L-1 答:(略)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com