
题目列表(包括答案和解析)
 随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定的精确度也越来越高.现有一种简单可行的测定方法,其具体操作步骤如下:
随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定的精确度也越来越高.现有一种简单可行的测定方法,其具体操作步骤如下:| 58.5×(V1-V2) |
| 2ma3 |
| 58.5×(V1-V2) |
| 2ma3 |

随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定精确度也越来越高.现有一简单可行的测定方法,具体步骤如下:①将固体食盐研细,干燥后,准确称取m g NaCl固体并转移到定容仪器A中 ②用滴定管向仪器A中加苯,并不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为V mL
回答下列问题:
(1)步骤①中A仪器最好用________(填仪器名称)
(2)能否用胶头滴管代替步骤②中的滴定管?其原因是________
(3)能否用水代替苯________________理由是________________
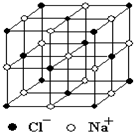
(4)已知NaCl晶胞的结构如图所示,经X射线衍射测得晶胞中最邻近的Na+和C1-平均距离为a cm,则利用上述方法测得的阿伏加德罗常数的表达式为NA=________.

(5)纳米材料的表面原子占总原子数的比例极大,这是它具有许多特殊性质的原因,假设某氯化钠纳米颗粒的大小和形状恰好等于氯化钠晶胞的大小和形状,则这种纳米颗粒的表面原子占总原子数的百分比为________.

NaCl晶体结构示意图
图1-1-1
(1)将固体NaCl细粒干燥后,准确称取m g NaCl固体并转移到定容仪器A中;
(2)用滴定管向A仪器中加苯,不断振荡,继续加苯至A仪器的刻度,计算出NaCl固体的体积V cm3。
请回答下列问题:
①步骤(1)中A仪器最好使用__________ (填序号)。
A.量筒 B.烧杯 C.容量瓶 D.试管
②步骤(2)中用酸式滴定管还是用碱式滴定管__________,理由是____________________。
③能否用水代替苯__________,理由是___________________________________________。
④已知NaCl晶体中,靠得最近的Na+与Cl-间的平均距离为a cm(如图1-1-1),用上述测定方法测得的阿伏加德罗常数NA的表达式为_________________________________________。
(3)另一种方法是电解法,方法是:用铂电极电解CuCl2溶液时,当电流为I,通电时间为t(单位:分钟)时,阴极增加的质量为m,在阳极收集到气体体积(标准状况)为V。又知1个电子的电荷量为Q,铜的摩尔质量为M,则计算阿伏加德罗常数NA的算式为( )
A.It/QV B.32It/mQ C.672It/QV D.30MIt/mQ
(4)由实验得知,用电解法将电解液中的金属离子还原为金属单质时,电极所通过的电量Q正比于金属的物质的量n和金属离子的化合价a的乘积,其比例系数F是一恒量,称为法拉第常数。它与金属的种类无关。
用电镀法在半径为R的铜球表面均匀镀上很薄的银层,在电解槽中铜球作__________极,另一电极材料是__________。若电流为I,通电时间为t,银的相对原子质量为A,金属银的密度为ρ,求镀层的厚度d(用本题中的符号表示)。
(15分)随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定的精确度也越来越高。现有一种简单可行的测定方法,其具体操作步骤如下:① 用分析天平称取研细干燥的NaCl固体![]() g于体积为V1毫升的定容容器A中;② 用滴定管向定容容器A中加入苯,并不断振荡,加苯到定容容器A的刻度线时所加入苯的体积为V2毫升;根据以上操作回答以下问题:
g于体积为V1毫升的定容容器A中;② 用滴定管向定容容器A中加入苯,并不断振荡,加苯到定容容器A的刻度线时所加入苯的体积为V2毫升;根据以上操作回答以下问题:
(1)定容容器A最好用________________(填实验仪器名称);
(2)滴定管是用酸式滴定管还是用碱式滴定管?_____________________,为什么?
______________________________________________________________;
(3)能否用水代替苯?_____________,为什么?
_______________________________________________________;
(4)测定离子化合物中离子间的间隔的方法是用X—射线衍射法,已知X—射线衍射仪测出的NaCl晶体中相邻Na+和Cl-的核间距为![]() cm。则利用上述方法测得的阿伏加德罗常数的数学表达式为:
cm。则利用上述方法测得的阿伏加德罗常数的数学表达式为:![]() ______________________;
______________________;
(5)纳米材料的表面原子占总原子数的比例极大,这是它具有许多特殊性质的原因,假设某纳米颗粒的大小和形状恰好等于氯化钠晶胞的大小和形状,则这种纳米颗粒的表面原子占总原子数的百分比为:______________。
一、选择题(本题共16个小题,每小题3分。每小题只有一个选项符合题意。)
题号
1
2
3
4
5
6
7
8
答案
D
C
D
D
B
A
D
D
题号
9
10
11
12
13
14
15
16
答案
B
B
A
C
B
D
B
D
|