
题目列表(包括答案和解析)
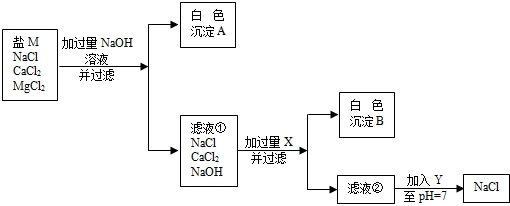
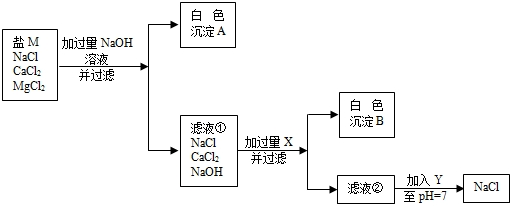

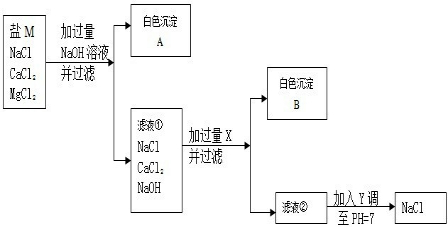
食盐在生产和生活中具有广泛的用途.
(1)去除粗盐中难溶性的杂质,主要实验步骤有:溶解、过滤、 .在过滤操作中,玻璃棒的作用是
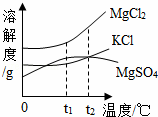
(2)晒盐场经常利用晾晒海水得到粗盐和卤水.卤水的主要成分及其溶解度的变化如图.
将t1℃时3种物质的饱和溶液升温到t2℃时,3种溶液溶质的质量分数由小到大的顺序是 .
(3)将纯净的氯化钠配制成溶液.20℃时,向4个盛有200g水的烧杯中,分别加入一定质量的氯化钠并充分溶解.4组实验数据如下:
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化钠的质量/g | 9 | 36 | 81 | 90 |
| 溶液质量/g | 209 | 236 | 272 | 272 |
若将①中得到的溶液稀释成质量分数为0.9%的生理盐水,需加水的质量是 g.
关于上述实验的叙述正确的是 (填序号).
a.①②所得溶液是不饱和溶液
b.③④所得溶液中,溶质的质量分数相等
c.20℃时,200g水中最多溶解氯化钠的质量为72g
d.20℃时,将④继续恒温蒸发100g水,过滤,得到质量为36g的固体.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com