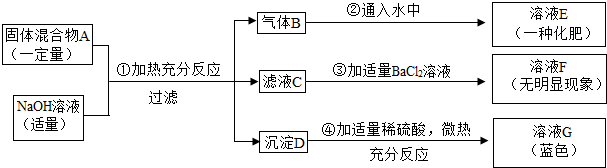
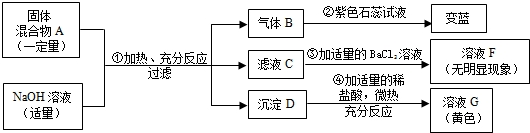
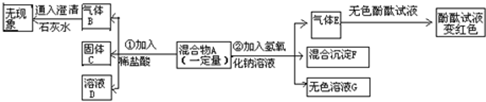
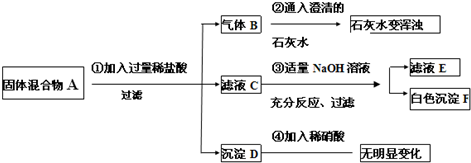
现欲探究一固体混合物A的成分,已知其中可能含有BaCl
2、Na
2CO
3、FeCl
3、Fe
2O
3四种物质中的两种或多种.按图所示进行实验.出现的现象如图中所述(设过程中所有可能发生的反应都恰好完全进行).
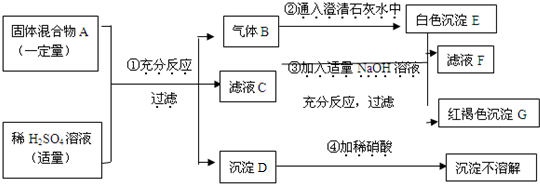
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)沉淀D的化学式为
BaSO4
BaSO4
.
(2)滤液F中大量存在的金属阳离子为(写离子符号)
Na+
Na+
.
(3)写出实验过程③中生成沉淀G所发生反应的化学方程式:
3NaOH+FeCl3═Fe(OH)3↓+3NaCl或6NaOH+Fe2(SO4)3═3Na2SO4+2Fe(OH)3↓
3NaOH+FeCl3═Fe(OH)3↓+3NaCl或6NaOH+Fe2(SO4)3═3Na2SO4+2Fe(OH)3↓
.
(4)混合物A中,肯定存在的物质是(写化学式)
BaCl2、Na2CO3
BaCl2、Na2CO3
.不能确定是否存在的物质是
FeCl3、Fe2O3
FeCl3、Fe2O3
,理由是
Fe2O3与硫酸反应生成硫酸铁也能与氢氧化钠溶液反应
Fe2O3与硫酸反应生成硫酸铁也能与氢氧化钠溶液反应
.