
题目列表(包括答案和解析)
| 操作步骤 | 现象 | 结论 |
| (1)取样加入足量CaCI2溶液 (2)再向溶液中滴加酚酞 |
有白色沉淀生成 有白色沉淀生成 |
样品溶液中含Na2CO3溶液 样品溶液中含Na2CO3溶液 |
溶液呈红色 溶液呈红色 |
样品溶液中含有NaOH 样品溶液中含有NaOH |
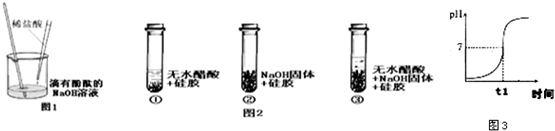
某研究性学习小组对中和反应进行探究,请你参与实验:
实验1:证明酸和碱发生了反应
稀盐酸和NaOH溶液混合没有明显现象,小丽同学按图1进行实验,证明了盐酸和
NaOH溶液发生化学反应,他依据的实验现象是 。

实验2:证明酸和碱反应有水生成
小明同学取变色硅胶(吸水后由蓝色变红色)、无水醋酸(一种酸,常温下为无色液体)和氢氧化钠固体进行图2所示的三个实验。
(1)加入试剂后,要迅速塞紧橡胶塞的目的是 。
(2)能证明酸和碱反应有水生成,依据的现象是 。
实验3:测量酸和碱反应过程的pH
(1)实验过程中用传感器实时获得溶液的pH,要得到如图所得变化曲线,所进行的操作是 (填字母)。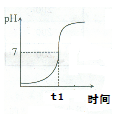
A.将盐酸溶液逐滴滴加到氢氧化钠溶液中
B.将氢氧化钠溶液爱滴滴加到盐酸溶液中
(2)0—t1时,溶液的酸碱性变化情况是_________________。根据图溶液pH的变化,判断酸和碱发生反应的依据是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com