
题目列表(包括答案和解析)
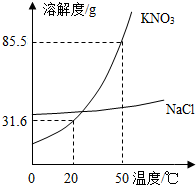 (2013?北辰区一模)实验室欲配制一定溶质质量分数的KNO3溶液,现只有含少量NaCl的KNO3固体样品.
(2013?北辰区一模)实验室欲配制一定溶质质量分数的KNO3溶液,现只有含少量NaCl的KNO3固体样品.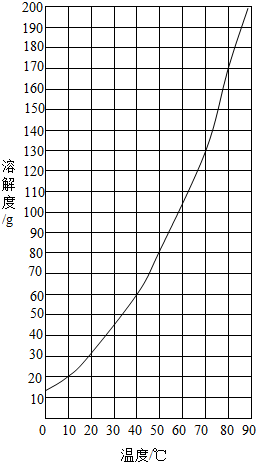 (2013?广州)实验室需配制一定浓度的硝酸钾溶液.
(2013?广州)实验室需配制一定浓度的硝酸钾溶液.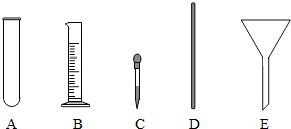
| 温度/℃ 质量分数/% |
20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com