
题目列表(包括答案和解析)


甲、乙两上实验小组分别进行测定Na2CO3和NaC1混合物中Na2CO3含量的实验。
甲组:沉淀分析法(相对分子质量:Na2CO3为106; BaCO3为197; BaCl2为208) (1)配制一定物质的量浓度的BaC12溶液:用已经称量好的 gBaC12固体配制0.4mol·L—lBaCl2溶液250 mL,所需要的仪器为量筒和 。
(1)配制一定物质的量浓度的BaC12溶液:用已经称量好的 gBaC12固体配制0.4mol·L—lBaCl2溶液250 mL,所需要的仪器为量筒和 。
(2)把m g混合物溶解后加入过量BaC12溶液,然后将所得沉淀过滤、洗涤、烘干、称量,固体质量为wg,根据沉淀质量计算原混合物中Na2CO3的质分数为 (用含m、w的代数式表示)。如果原溶液中过量的Ba2+浓度达到0.01mol/L,则溶液中残留的CO32—的物质的量浓度是 。
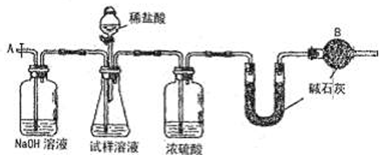
乙组:气体分析法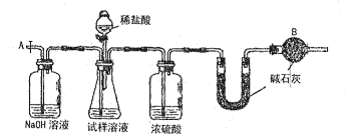
(3) 实验中待锥形瓶中不再产生气体后,打开活塞从导管A端缓缓鼓入一定量的空气,这样做的目的是 。
实验中待锥形瓶中不再产生气体后,打开活塞从导管A端缓缓鼓入一定量的空气,这样做的目的是 。
(4)装置中干燥管B的作用是 。
(5)除已理的agNa2CO3样品外,实验中还应测定的数据是 处(填图中仪器的名称)装置实验前后的质量差。
(6)该实验还存在的明显缺 陷是 。
陷是 。
 (1)配制一定物质的量浓度的BaC12溶液:用已经称量好的 gBaC12固体配制0.4mol·L—lBaCl2溶液250 mL,所需要的仪器为量筒和 。
(1)配制一定物质的量浓度的BaC12溶液:用已经称量好的 gBaC12固体配制0.4mol·L—lBaCl2溶液250 mL,所需要的仪器为量筒和 。
 实验中待锥形瓶中不再产生气体后,打开活塞从导管A端缓缓鼓入一定量的空气,这样做的目的是 。
实验中待锥形瓶中不再产生气体后,打开活塞从导管A端缓缓鼓入一定量的空气,这样做的目的是 。 陷是 。
陷是 。湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com