
题目列表(包括答案和解析)
(15分)焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用右图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5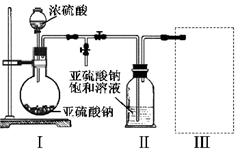
(1)装置I中产生气体的化学方程式为 。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为 (填序号)。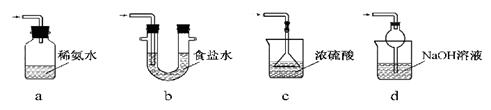
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO3- 的电离程度大于水解程度,可采用的实验方法是 (填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸
d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是 。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”“偏低”或“不变”)。



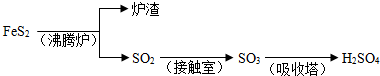
肼(N2H4)又称联氨,是一种可燃性液体,与氧气或氮氧化物反应均可生成氮气和水.氢气是一种清洁能源,液氢和肼均可用作火箭燃料.
Ⅰ氢气的制取与储存是氢能源利用领域的研究热点.
已知:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH=+247.4 kJ·mol-1
(1)氢气作为新能源的优点________.(答2点)
(2)以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为________.
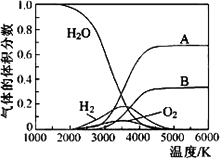
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图所示.图中A、B表示的物质依次是________、________.
Ⅱ(4)肼一空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,负极的电极反应式是________.
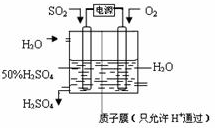
(5)下图是一个电化学装置示意图.用肼一空气燃料电池做此装置的电源.
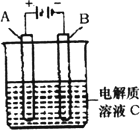
①如果A是铂电极,B是石墨电极,C是硫酸-硫酸铵,阴极的电极反应式是________.
②利用该装置可制得少量过氧化氢:在阳极上SO42-被氧化成S2O82-(过二硫酸根离子),S2O82-与H2O反应生成H2O2,S2O82-+2H2O=2SO42-+H2O2+2H+.若要制取2 molH2O2,该燃料电池理论上需消耗________molN2H4.
(6)由A、B、C、D四种金属按下表中装置进行实验.
实验装置与现象
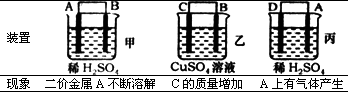
根据实验现象回答下列问题:
①装置丙中溶液的PH________.(填“变大”“变小”或“不变”)
②四种金属活泼性由弱到强的顺序是________.

| 1 |
| 2 |
| ||
| △ |
| T/K | 673 | 723 | 823 | 923 |
| K | 423 | 37.4 | 20.5 | 4.68 |
| ||
| 高温 |
| 浓硫酸 |
| 浓硫酸 |
| 铁屑 |
| 铁粉 |
| 高温 |
| 浓硫酸 |
一、二、选择题
题号
1
2
3
4
5
6
7
8
9
答案
A
B
D
C
B
C
A
D
C
题号
10
11
12
13
14
15
16
17
18
答案
AC
BD
BD
B
A
CD
D
BD
C
三、本题包括3小题,共33分
19.(10分)⑴CO2+NH3+NaCl+H2O=NaHCO3↓+ NH4Cl(2分)
⑵ ①稀盐酸挥发出的氯化氢气体也被氢氧化钠溶液吸收; (1分)
②烧瓶和导管中滞留的二氧化碳气体不能被氢氧化钠溶液吸收. (1分)
⑶①关闭酸式滴定管活塞,用手捂热烧瓶,若注射器活塞外移,松手后回到原来位置,说明气密性良好(1分)

(2分)
⑷①减少二氧化碳在水中的溶解,减小实验误差(1分)
②读数前将广口瓶与量筒之间导管中的水转入量筒;(1分)读取量筒中水的体积时要平视(1分)
20.(12分)⑴SO2 (g) + O2(g)
O2(g) SO3(g);△H ? 98.3 kJ/mol(2分)
⑵提高二氧化硫的转化率(2分)
⑶

 给催化剂加热(1分) 因为该反应为放热反应,这样做是为了防止温度过高,而使SO2的转化率和催化剂的活性降低(2分)
给催化剂加热(1分) 因为该反应为放热反应,这样做是为了防止温度过高,而使SO2的转化率和催化剂的活性降低(2分)
⑷ 或 × 100%(2分)
⑸(3分)
 21.(共11分)
21.(共11分)
I.⑴ 2Cu(NO3)2 2CuO+4NO2↑+O2↑(2分)
 ⑵正确,(1分)2Cu(NO3)2分解产生的混合气体中O2的体积分数与空气中O2的体积分数相当空气中带火星的木条不复燃,而在NO2和O2混合气体中木条复燃,所以NO2能支持燃烧。(2分)
⑵正确,(1分)2Cu(NO3)2分解产生的混合气体中O2的体积分数与空气中O2的体积分数相当空气中带火星的木条不复燃,而在NO2和O2混合气体中木条复燃,所以NO2能支持燃烧。(2分)
Ⅱ.⑴ 4HNO3浓 4NO2↑+O2+2H2O(2分)
⑵不正确。(1分)带火星的木条熄灭可能是由于加热时产生大量水蒸气所致。(1分)
Ⅲ.用Cu与浓HNO3反应制取NO2气体,并用浓H2SO4干燥,再将带火星的木条伸入NO2中观察现象。(2分)
四.(本题包括3小题,共33分)
22.(共10分)
⑴ (1)A ⑵CD ⑶熟石灰(1分) 2CaSO4? H2O+3H2O===2CaSO4?2H2O(2分)
H2O+3H2O===2CaSO4?2H2O(2分)
⑷S=C=O(2分)
⑸ NH3+HCl===NH4Cl(2分)
23.(10分)
⑴HClO4>H2SO4>H2CO3(2分)
⑵N2H4+4OH--4e-=N2↑+4H2O(2分)
|