
题目列表(包括答案和解析)
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | ||||||||||||||||


| ||
| 8NAd3 |
| ||
| 8NAd3 |
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | J | K | L | ||||||||||||
| M | N | ||||||||||||||||


| ||
| ||
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 | |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- |
K1=4.31×10-7 K2=5.61×10-11 |
|
| C6H5OH | C6H5OH?C6H5O-+H+ | 1.1×10-10 | |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
|
| NH3?H2O | NH3?H2O?NH4++OH- | 1.76×10-5 | |
| BaSO4 | BaSO4?Ba2++SO42- | 1.07×10-10 | |
| BaCO3 | BaCO3?Ba2++CO32- | 2.58×10-9 |
| 族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | A | ||||||
| 2 | B | C | D | E | J | K | L |
| 3 | F | G | H | I | |||
| M |
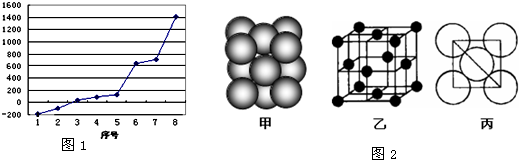
 它的空间利用率为
它的空间利用率为一、二、选择题
题号
1
2
3
4
5
6
7
8
9
答案
A
B
D
C
B
C
A
D
C
题号
10
11
12
13
14
15
16
17
18
答案
AC
BD
BD
B
A
CD
D
BD
C
三、本题包括3小题,共33分
19.(10分)⑴CO2+NH3+NaCl+H2O=NaHCO3↓+ NH4Cl(2分)
⑵ ①稀盐酸挥发出的氯化氢气体也被氢氧化钠溶液吸收; (1分)
②烧瓶和导管中滞留的二氧化碳气体不能被氢氧化钠溶液吸收. (1分)
⑶①关闭酸式滴定管活塞,用手捂热烧瓶,若注射器活塞外移,松手后回到原来位置,说明气密性良好(1分)

(2分)
⑷①减少二氧化碳在水中的溶解,减小实验误差(1分)
②读数前将广口瓶与量筒之间导管中的水转入量筒;(1分)读取量筒中水的体积时要平视(1分)
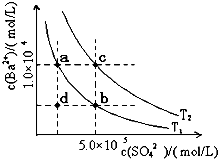
20.(12分)⑴SO2 (g) + O2(g)
O2(g) SO3(g);△H ? 98.3 kJ/mol(2分)
⑵提高二氧化硫的转化率(2分)
⑶

 给催化剂加热(1分) 因为该反应为放热反应,这样做是为了防止温度过高,而使SO2的转化率和催化剂的活性降低(2分)
给催化剂加热(1分) 因为该反应为放热反应,这样做是为了防止温度过高,而使SO2的转化率和催化剂的活性降低(2分)
⑷ 或 × 100%(2分)
⑸(3分)
 21.(共11分)
21.(共11分)
I.⑴ 2Cu(NO3)2 2CuO+4NO2↑+O2↑(2分)
 ⑵正确,(1分)2Cu(NO3)2分解产生的混合气体中O2的体积分数与空气中O2的体积分数相当空气中带火星的木条不复燃,而在NO2和O2混合气体中木条复燃,所以NO2能支持燃烧。(2分)
⑵正确,(1分)2Cu(NO3)2分解产生的混合气体中O2的体积分数与空气中O2的体积分数相当空气中带火星的木条不复燃,而在NO2和O2混合气体中木条复燃,所以NO2能支持燃烧。(2分)
Ⅱ.⑴ 4HNO3浓 4NO2↑+O2+2H2O(2分)
⑵不正确。(1分)带火星的木条熄灭可能是由于加热时产生大量水蒸气所致。(1分)
Ⅲ.用Cu与浓HNO3反应制取NO2气体,并用浓H2SO4干燥,再将带火星的木条伸入NO2中观察现象。(2分)
四.(本题包括3小题,共33分)
22.(共10分)
⑴ (1)A ⑵CD ⑶熟石灰(1分) 2CaSO4? H2O+3H2O===2CaSO4?2H2O(2分)
H2O+3H2O===2CaSO4?2H2O(2分)
⑷S=C=O(2分)
⑸ NH3+HCl===NH4Cl(2分)
23.(10分)
⑴HClO4>H2SO4>H2CO3(2分)
⑵N2H4+4OH--4e-=N2↑+4H2O(2分)
|