
题目列表(包括答案和解析)
电解原理在化学工业中有着广泛的应用。右图是一个电解池,a为电解液,x和y是两块电极板,通过导线与直流电源相连。回答下列问题,
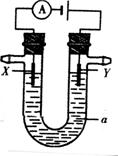
(1)若X 和Y 为惰性电极,a 为饱和的氯化钠溶液,则电解池中Y电极反应式 __________________________,检验该电极反应产物的方法是_______________________________________________________。
(2)若X 和Y分别为石墨和铁,a 为饱和的氯化钠溶液,则点解过程中生成地 白色固体物质为________________________。将该物质露置在空气中,可观察到得现象为
__________________________________________________________。
(3)某同学做该实验时用铅蓄电池做电源,已知铅蓄电池的工作原理为Pb + PbO2 +2H2SO4![]() 2PbSO4+2H2O,则该蓄电池的负极反应式为_______________________________.
2PbSO4+2H2O,则该蓄电池的负极反应式为_______________________________.
若反应过程中转移的电子为0.1mol,则反应中电池内消耗的硫酸为______________.
电解原理在化学工业中有着广泛的应用。如图表示一个电解池,装有电解液a, X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是 。在X极附近观察到的现象是 、 。
②Y电极上的电极反应式是 ,检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式是 。
②Y电极的材料是 ,电极反应式是 。(说明:杂质发生的电极反应不必写出)
电解原理在化学工业中有着广泛的应用。如图表示一个电解池,装有电解液a, X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是 。在X极附近观察到的现象是 、 。
②Y电极上的电极反应式是 ,检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式是 。
②Y电极的材料是 ,电极反应式是 。(说明:杂质发生的电极反应不必写出)

| A.若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液 |
| B.按图甲装置用惰性电极电解AgNO3溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 |
| C.按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5 mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol |
| D.若X、Y为铂电极,a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol·L-1 |
电解原理在化学工业中有着广泛的应用.
现将你设计的原电池通过导线与下图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:
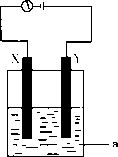
①若X和Y均为惰性电极,a为CuSO4溶液则阳极的电极反应式为________,电解时的化学反应方程式为________,通过一段时间后,向所得溶液中加入0.2 mol CuO粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为________.
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电极反应式为________
③若用此装置电解精炼铜,________做阳极,电解液CuSO4的浓度________(填“增大”、“减小”或“不变”).
④若用此装置在铁制品上镀铜,铁制品做________,电镀液的浓度________(填“增大”、“减小”或“不变”).
1.A(碘单质遇淀粉变蓝色,而不是碘酸钾)
2.D(同温同压下,mg气体A与ng气体B的分子数目相同,说明物质的量相同,A、B、C正确,D同温同压下,气体A与气体B的密度之比等于它们的物质的量之比为m : n)
3.C(从③处导出的气体含有少量SO2、O2 、N2等,不可直接排入大气,否则造成污染)
4.A(B项由于不知道气体的状态,
5.A(放出热量ΔH<0,所以A错误;其它说法均正确)
6.A(水的热稳定性比较高是因为水分子中氢氧键的键能大;金属晶体导电是因为含有自由移动的电子;离子晶体硬度较大、难于压缩是因为离子键键能大)
7.D (D中上下移动时,两端液面始终平衡说明装置漏气)
8.B(过氧化钠固体与水反应,是放热反应,A、C错误;放热使广口瓶中气体温度升高膨胀,则右边升高左边下降)
9.A(ClO-+2I-+2H+===Cl-+I2+H2O;SO+I2+H2O===2I-+SO+2H+,所以可知氧化性为:ClO->I2>SO,因为②中加入过量的Na2SO3 溶液,所以③中含有BaSO3沉淀;①中硫酸只起到酸性作用,②只能证明SO有还原性)
10.C(二元弱酸应分步电离;草酸滴定KMnO4属于氧化还原滴定,不用指示剂;乙二酸脱水分解产物是CO、CO2和H2O)
11.A((NH4)2SO4和CH3COOH明显属于电解质;Cl2是单质既不属于电解质也不属于非电解质;虽然NH3的水溶液能够导电,那是由于生成了一水合氨的原因,故NH3属于非电解质。)
12.D(CsCl和NaCl的阴、阳离子排列方式不同;金属晶体中只有阳离子,没有阴离子;分子晶体中不一定含有共价键如稀有气体)
13.D(①说明有Br-、CO,有CO就没有Fe2+②说明没有SO③说明没有I-)
14.D(能发生这两个电极反应的可能是原电池,也可能是电解池,如果是原电池,则b为铁电极,a为没铁活泼的金属或非金属做电极,电解溶液为含铜离子的溶液;如果是电解池,b用铁做电极和电源的正极相连,a可以和铁相同的电极也可以不同,溶液为含铜离子的溶液)
15.C(A称量时应左物右码,B配制150mL0.10mol/L溶液应用150mL的容量瓶,而且要用玻璃棒引流;D冷凝水的方向应从下进上出)
16.D(①所取浓硫酸的体积少,②③④均造成溶质的损失)
17.问题1:(1)合成氨工业 硫酸工业(其他合理答案也正确) (2分)
问题2:Cu+4H++2NO(浓)===Cu2++2NO2↑+2H2O
3Cu+8H++2NO(稀)===3Cu2++2NO↑+4H2O(其他合理答案也正确)(2分)
化学?第页(见反面)问题3:放热 C(金刚石、s)=C(石墨、s);ΔH=-1.90kJ/mol(2分)
问题4:(1)第二个反应为:Al3++3OH-===Al(OH)3↓ (2分)
(2)最后一个离子反应为:Al(OH)3+OH-===AlO+2H2O (2分)
问题5:4KMnO4+5KI+7H2SO4===4MnSO4+I2+3KIO3+3K2SO4+7H2O (2分) (其他合理答案也正确)
18.(1)①2Cl--2e-=Cl2↑(2分) 用湿润的淀粉-KI试纸靠近Y极支管口(其它合理答案均可)(2分)
②由于2H++2e-=H2↑ 放出氢气,使水的电离平衡向正反应方向移动,使c(OH-)不断增大,所以pH会增大(2分)
③先有白色沉淀生成,继而变成灰绿色,最后变成红褐色(2分)
(2)①A(1分) ②B(1分)
19.(每空2分)(1)NaI NaClO
(2)2I-+ClO-+H2O===I2+Cl-+2OH- I2+5ClO-+2OH-===2IO+5Cl-+H2O
(3)Cl2+2NaOH===NaClO+NaCl+H2O
20.(1)KClO3 (1分) H????????H(1分)
(2)①关闭分液漏斗活塞,在II中加水,没过长导管口,用酒精灯微热圆底烧瓶,若II中有气泡冒出,停止加热后,有水进入II中的长导管,形成一段稳定的水柱,则证明I气密性良好。 (或用止水夹夹住c处,向分液漏斗中加水,打分液漏斗的活塞,若分液漏斗中的水不再下流,则证明I气密性良好。)(2分)
②MnO2+4H++2Cl-Mn2++Cl2↑+2H2O(2分)
③S2-+Cl2===S↓+2 Cl-(2分)
化学?第页 ④II III(1分) 除去氯气中的水蒸气(或干燥氯气)(1分)
(3)Cl2+H2O2===2HCl+O2(2分)
21.(1)7Cl2+14NaOH===9NaCl+4NaClO+NaClO3+7H2O
(2)C(NaCl)=1.8mol/L,Cl(NaClO)=0.8mol/L,C(NaClO3)=0.2mol/L (每个2分)
解析:解答此题的关键是第(1)问.可根据得失电子数相等确定生成物NaCl、NaClO、NaClO3的物质的量之比,进而确定化学方程式中化学计算数.
(1)依题意可设生成NaClO的物质的量为4mol,NaClO3的物质的量为1mol,设生成NaCl的物质的量x,根据得失电子的物质的量相等,有:1×x=1×4mol+5×1mol,解得:x=9mol.
NaCl、NaClO、NaClO3化学计量数之比与生成对应物质的物质的量相等,即等于9∶4∶1.据此可写出总的化学字方程式:7Cl2+14NaOH===9NaCl+4NaClO+NaClO3+7H2O
(2)n(Cl2)=
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com