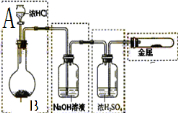
为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:在不加热的情况下用右图装置制取氯气,已知A是HCl,B为固体,则B可能是
高锰酸钾
高锰酸钾
(写物质名称,任写一种即可),该反应的化学方程式为:
2KMnO4+8HCl=2MnCl2+2KCl+Cl2↑+4H2O
2KMnO4+8HCl=2MnCl2+2KCl+Cl2↑+4H2O
实验二:用图除去氯气中的杂质,洗气装置内的洗涤液一般用
饱和食盐水、浓硫酸
饱和食盐水、浓硫酸
溶液.某同学用图装置为了获得较大浓度的氯水,他将进气导管末端连一多孔的球泡,在装置右边气体出口导管处连一干瘪的橡皮气囊,请说明理由:
增大气体与溶液的接触面积,使反应充分进行,氯气有毒污染空气,防止氯气排放,橡皮气囊起到储存气体,平衡压强
增大气体与溶液的接触面积,使反应充分进行,氯气有毒污染空气,防止氯气排放,橡皮气囊起到储存气体,平衡压强
.
实验三:将制得的氯水转移到锥形瓶中,再加入大理石,并充分振荡,观察到氯水的黄绿色褪去,同时产生少量气体.分别取锥形瓶中上层清液4份,进行如下实验,请用化学式填空:
(1)该清液滴在有色布条上有极强的漂白作用.说明该清液中含有
HClO
HClO
(写化学式);
(2)该清液中滴加碳酸钠溶液产生白色沉淀.说明该清液中含有
Ca2+
Ca2+
离子;
(3)该清液中滴加盐酸可产生大量气体.该气体是
CO2
CO2
;
(4)该清液加热后变浑浊并产生大量气体.加热后产生浑浊的原因是因为生成了
CaCO3
CaCO3
.
(5)通过上述实验,请写出氯水和碳酸钙反应的化学方程式为:
2CaCO3+2Cl2+H2O=CaCl2+Ca(HCO3)2+2HClO
2CaCO3+2Cl2+H2O=CaCl2+Ca(HCO3)2+2HClO
.

 为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:


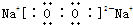
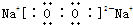
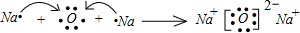
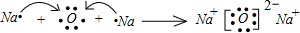

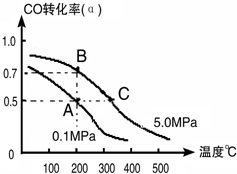
 CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.
CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.