
题目列表(包括答案和解析)
|
有关溶度积Ksp的说法正确的是 | |
| [ ] | |
A. |
Ksp的数值只与温度有关 |
B. |
Ksp的数值只与难溶电解质的性质和温度有关 |
C. |
Ksp的大小与沉淀量有多少和溶液中离子浓度的大小有关 |
D. |
Ksp的数值越大,电解质在水中的溶解能力越强 |
下列说法正确的是
A.已知Ag2CrO4的Ksp为1.12×10-12,则将等体积的1×10-3mo1/L的AgNO3溶液和1×0-3mo1/LK2CrO4溶液混合,会有Ag2CrO4沉淀产生
B.Si—O键的键能大于Si—Cl键的键能,因此SiO2的熔点高于晶体SiCl4的熔点
C.常温时,浓度均为0.01mol/L Na2CO3溶液和NaHCO3溶液,等体积混合,其溶液中粒子浓度关系为3c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3)
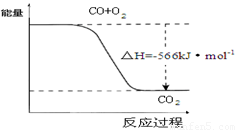
D.已知:2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1,下图可表示由CO生成CO2的反应过程和能量关系
下列说法正确的是
| A.已知Ag2CrO4的Ksp为1.12×10-12,则将等体积的1×10-3mo1/L的AgNO3溶液和1×0-3mo1/LK2CrO4溶液混合,会有Ag2CrO4沉淀产生 |
| B.Si—O键的键能大于Si—Cl键的键能,因此SiO2的熔点高于晶体SiCl4的熔点 |
| C.常温时,浓度均为0.01mol/L Na2CO3溶液和NaHCO3溶液,等体积混合,其溶液中粒子浓度关系为3c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3) |
| D.已知:2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1,下图可表示由CO生成CO2的反应过程和能量关系 |

下列说法正确的是
| A.常温下,某溶液中由水电离出的c(H+)=1×10-amo1·L–1,若a<7时,则该溶液可能为NaHSO4溶液 |
| B.常温下,中和同体积、同pH的硫酸、盐酸和醋酸所需相同浓度的NaOH溶液的体积关系:V(硫酸)>V(盐酸)=V(醋酸) |
| C.25℃时,已知Ka(CH3COOH)=1.7×10-5mo1·L–1、Ka(C6H5OH) =1.0×10-10mo1·L–1、 Ka1(H2CO3) = 4.2×10-7mo1·L–1 、Ka2(H2CO3) =5.6×10-11mo1·L–1pH相等的①CH3COONa ②C6H5ONa ③NaHCO3溶液中,c(Na+)大小关系:②<③<① |
| D.常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加入稀盐酸有气泡产生,说明常温下Ksp(BaSO4)>Ksp(BaCO3) |
下列说法正确的是
| A.水的离子积常数KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度 |
| B.Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关 |
| C.常温下,向10mL PH=3的醋酸溶液中加水稀释后,溶液中C(CH3COO--)/C(CH3COOH) C(OH--)的值减小 |
| D.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,c(NH)/c(NH3·H2O)的值增大 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com