
题目列表(包括答案和解析)
| ||
| ||
| ||
| ||
| 压强/Mpa 转化率 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
A.![]() t B.
t B.![]() t
t
C.![]() t D.
t D.![]() t
t
(1)在接触室中生成SO3的反应条件的选择,可以完全用勒夏特列原理解释的是 。?
A.用V2O5作催化剂? B.温度为400~500 ℃? C.常压? D.O2过量?
(2)在硫酸工业的尾气中, 是主要的大气污染物,必须进行净化处理,处理方法可采用过量氨水吸收,反应的离子方程式是 。?
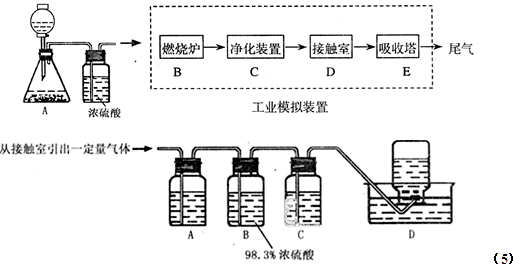
(3)下图是工业制取硫酸的三个主要设备,写出A装置的名称 ;写出B中发生的反应的化学方程式: 。?

(4)现有含FeS272%的黄铁矿100吨,如果在煅烧的过程中,FeS2损失了10%,则可生成质量分数为98%的硫酸 吨。?
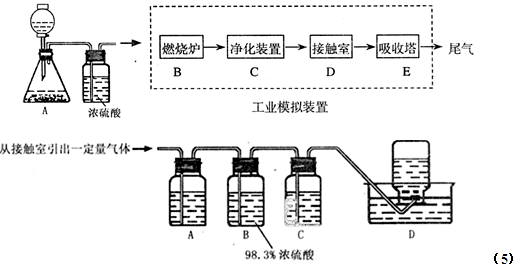
某化学兴趣小组的同学为模拟工业制造硫酸的生产过程,设计了如图所示的装置,请根据根据回答问题:
(1)装置A用来制取氧气,写出相应的化学方程式 ;

(2)燃烧炉内放一定量黄铁矿粉末,在高温条件下和A装置制出的氧气充分反应,其化学方程式为 ;现有含FeS260%的黄铁矿100t,如果在煅烧的过程中,S损失了18%,则可生产质量分数为98%的硫酸 吨。
(3)C装置为净化装置,若无该装置,将混合气体直接通入D装置,除对设备有腐蚀外,还会造成的后果是 ;
(4)工业上利用2SO2(g)+O2(g)====2SO3(g)反应制备SO3,下表是在一定条件下测定的SO2的转化率,根据表格中提供的数据,请选择工业利用该反应制备SO3的温度与压强 。
|
转化率 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(5)为检验从接触室出来的气体成分,甲同学设计如下实验:

①A中盛放的试剂是 ;
②B中盛放98.3%浓硫酸的作用是 ,乙同学提出可用饱和NaHSO3溶液代替98.3%的浓硫酸,请你判断乙同学的方案 (填“可行”或“不可行”说明理由 ;
③C中盛放的试剂是 ,其作用是 ;
(6)在硫酸工业的尾气中,SO2是主要大气污染物,必须进行净化处理,处理方法可采用过量氨不吸收,反应的离子方程式是 。
| 压强/Mpa 转化率 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com