
题目列表(包括答案和解析)
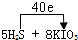
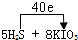
I.(1)请将反应物的化学式及配平后的系数填入下列相应的位置中:
FeSO4+HNO3→Fe(NO3)3+Fe2(SO4)3+N2O↑+________
(2)反应物中发生还原反应的物质________,被还原的元素是________.
(3)反应中1mol还原剂________(填“得到”或“失去”)________mol电子.
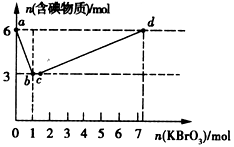
II.已知2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-
(1)若向FeI2和FeBr2混合液中通入过量氯气,写出可能发生的离子方程式________.
(2)若向含amolFeI2和bmolFeBr2混合液中通入cmol氯气,当I-、Fe2+、Br-完全被氧化时,c为________mol(用含a,b的式子表示)
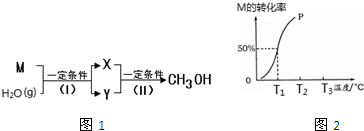
 2HI(g),实验测得起始及平衡时的有关数据如表所示:
2HI(g),实验测得起始及平衡时的有关数据如表所示: 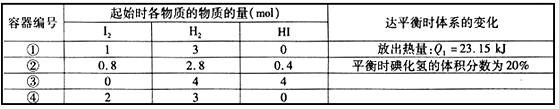
 2HI(g) △H=-23.15kJ/mol
2HI(g) △H=-23.15kJ/mol 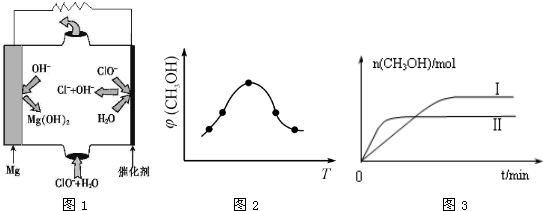
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com