
题目列表(包括答案和解析)
(1)常温下将气体B通入水中发生反应,生成A和D,则D的化学式为_________________。
(2)E分子的空间构型是_______________________;写出E与氧气反应生成A的化学方程式_______________________________________________。
(3)写出工业合成E反应的化学方程式______________________________________________。
若使该平衡向生成E的方向移动,可采取的措施有(填字母序号)__________________。
A.升高温度 B.增大压强
C.使用催化剂 D.液化分离E
(4)D和E生成的化合物在某温度下加热分解,同时生成两种氧化物。且在此过程中,若有0.5 mol该化合物完全反应,转移电子数为2 mol。写出该反应的化学方程式__________________
_____________________________________________________________________。
| |||||||||||||||||||
A、B、C、D、E为含同一种元素的常见物质.C物质只由一种元素组成,在1个C分子中形成共价键的电子数与分子中所含电子数之比为3∶7.C、E均可与氧气在一定条件下反应生成A.请回答以下问题:
(1)常温下将气体B通入水中发生反应,生成A和D,则D的化学式为________;
(2)E分子的空间构型是________;写出E与氧气反应生成A的化学方程式________;
(3)写出工业合成E反应的化学方程式________;
若使该平衡向生成E的方向移动,可采取的措施有(填字母序号)________;
A.升高温度
B.增大压强
C.使用催化剂
D.液化分离E
(4)D和E生成的化合物在某温度下加热分解,同时生成两种氧化物.且在此过程中,若有0.5 mol该化合物完全反应,转移电子数为2 mol.写出该反应的化学方程式________.
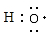

| A | C | |
| B |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com