
题目列表(包括答案和解析)
在常温下某化合物的水溶液中,已知由水电离出来的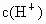 和
和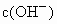 分别为
分别为 和
和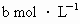 且
且 下列离子组在该溶液中一定能大量共存的是
下列离子组在该溶液中一定能大量共存的是
[ ]
A. 、
、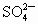 、
、 、
、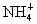
B.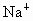 、
、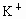 、
、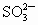 、
、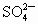
C.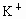 、
、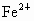 、
、 、
、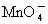
D.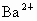 、
、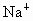 、
、 、
、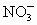
在常温下某化合物的水溶液中,已知由水电离出来的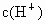 和
和 分别为
分别为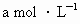 和
和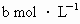 且
且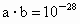 下列离子组在该溶液中一定能大量共存的是
下列离子组在该溶液中一定能大量共存的是
[ ]
A. 、
、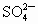 、
、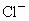 、
、
B.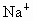 、
、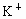 、
、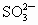 、
、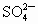
C.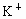 、
、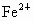 、
、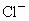 、
、
D.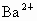 、
、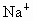 、
、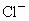 、
、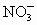
常温下某化合物的水溶液中,已知由水电离出来的c (H+)和c(OH-)分别为:a mol?L-1 和b mol ? L-1 ,且 a?b =10-28 ,下列离子组在该溶液中一定能大量共存的是 ( )
A.Al3+、 NH4+、 SO42-、 Cl- B.Na+、 K 十、SO42-、SO32一
C.K 十、 Mg2+、 Cl-、 MnO4- D.Ba2+、 Na+、 Cl- 、 NO3一
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com