
题目列表(包括答案和解析)
氧化还原反应中实验上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3―+4H++3e―→NO↑+2H2O;KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原反应过程发生。
(1)写出并配平该氧化还原反应的离子方程式:
(2)反应中硝酸体现了 和 性质。
(3)反应中若产生0.5mol气体,则转移电子的物质的量是 mol
(4)若1mol甲与某浓度硝酸反应时,和(1)反应相比被还原硝酸的物质的量增加,原因是: 。
Ⅰ⑴玻璃棒是中学化学实验中常用的仪器。下列过程中,一般不需要玻璃棒的是 ( 填写编号 )
①用PH试纸测定Na2CO3溶液的PH
②配制一定物质的量浓度的氯化钠溶液
③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体
④探究Ba(OH)2?8H2O晶体和NH4Cl晶体反应过程中的能量变化。
⑤实验室用新制备的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
⑵用“大于”“等于”“小于”填空
① 读量筒中液体的体积时,视线偏高,读取的体积数 实际体积数
② 用托盘天平称取10.4g食盐,将砝码和食盐的位置颠倒,所称食盐的质
量 10.4g
③配制500ml 0.1mol/lNaOH溶液,定容时俯视刻度线,所得溶液的物质的量浓
度 0.1mol/l
④用中和滴定法测某NaOH溶液的浓度,量取待测液未用该溶液润洗滴定管,测得的溶液的浓度 实际浓度
Ⅱ、氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:![]()
![]()
![]() 、
、![]() 、
、![]() 、
、![]()
![]() 四种物质中的一种物质能使上述还原过程发生。
四种物质中的一种物质能使上述还原过程发生。
(1)写出该氧化还原反应的方程式(不配平): 。
(2)该反应中氧化剂和还原剂物质的量之比为 。
(3)反应中硝酸体现了 、 性质。
(4)反应中若产生0.1mol气体,则转移电子的物质的量是 。
| B | ||
| A | X | C |
| D |
高一新教材中有一演示实验,用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来。
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:
第一,有氧气生成,第二, 。Na2O2跟水反应的化学方程式是 ,
其中还原剂是 ,氧化剂是 。
(2)某研究性学习小组拟用A图所示装置(气密性良好)进行实验,以证明上述结论。用以验证第一条结论的实验方法是:
用以验证第二条结论的实验方法是:
(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色。为探究其原因,该小组同学从查阅有关资料中得知:Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性。请设计一个简单的实验,验证Na2O2跟足量水充分反应后的溶液中有H2O2存在。(只要求写出实验所用的试剂及观察到的现象)
试剂: 。
现象: 。
(4)该小组同学提出用定量的方法探究Na2O2跟水反应后的溶液中否含有H2O2,其实验方法为:称取2.6g Na2O2固体,使之与足量的水反应,测量产生O2的体积并与理论值比较,即可得出结论。
|
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的(忽略导管在量筒中所占的体积) (填序号),理由是 。
②若在标准状况下测量气体的体积,应选用的量筒的大小规格为
(选填“100mL”“200mL”“500mL”或“1000mL”)。
用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,
观察到脱脂棉剧烈燃烧起来.
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:第一,有氧气生成;第二,_________.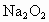 跟水反应的化学方程式是
跟水反应的化学方程式是
___________,其中还原剂是____________,氧化剂是_____________.
(2)某研究性学习小组拟用图所示装置(气密性良好)进行实验,以证明上述结论.用以验证第一条结论的实验方法是:_____________________.
用以验证第二条结论的实验方法是:__________________________.

(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色.为探究其原因,该小组同学查阅有关资料得知: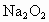 与水反应可生成
与水反应可生成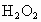 ,
,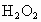 具有强氧化性和漂白性.请设计一个简单的实验,验证
具有强氧化性和漂白性.请设计一个简单的实验,验证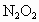 跟足量水充分反应后的溶液中有
跟足量水充分反应后的溶液中有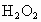 存在.(只要求写出实验所用的试剂及观察到的现象)
存在.(只要求写出实验所用的试剂及观察到的现象)
试剂:_______________________________________.
现象:_______________________________________.
(4)该小组同学提出用定量的方法探究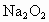 跟水反应后的溶液中是否含有
跟水反应后的溶液中是否含有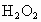 ,其实验方法为:称取2.6g
,其实验方法为:称取2.6g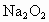 固体,使之与足量的水反应,测量产生
固体,使之与足量的水反应,测量产生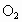 的体积并与理论值比较,即可得出结论.
的体积并与理论值比较,即可得出结论.
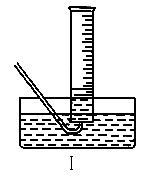
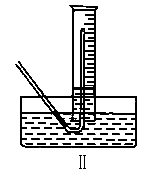
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的(忽略导管在量筒中所占的体积)________(填序号),理由是____________.
②若在标准状况下测量气体的体积,应选用的量筒的大小规格为________(选填“100mL”、“200mL”、“500mL”或“1000mL”).
用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,
观察到脱脂棉剧烈燃烧起来.
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:第一,有氧气生成;第二,_________.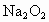 跟水反应的化学方程式是
跟水反应的化学方程式是
___________,其中还原剂是____________,氧化剂是_____________.
(2)某研究性学习小组拟用图所示装置(气密性良好)进行实验,以证明上述结论.用以验证第一条结论的实验方法是:_____________________.
用以验证第二条结论的实验方法是:__________________________.
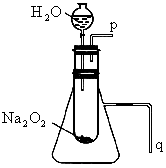
(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色.为探究其原因,该小组同学查阅有关资料得知: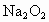 与水反应可生成
与水反应可生成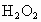 ,
,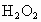 具有强氧化性和漂白性.请设计一个简单的实验,验证
具有强氧化性和漂白性.请设计一个简单的实验,验证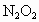 跟足量水充分反应后的溶液中有
跟足量水充分反应后的溶液中有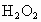 存在.(只要求写出实验所用的试剂及观察到的现象)
存在.(只要求写出实验所用的试剂及观察到的现象)
试剂:_______________________________________.
现象:_______________________________________.
(4)该小组同学提出用定量的方法探究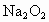 跟水反应后的溶液中是否含有
跟水反应后的溶液中是否含有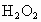 ,其实验方法为:称取2.6g
,其实验方法为:称取2.6g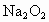 固体,使之与足量的水反应,测量产生
固体,使之与足量的水反应,测量产生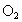 的体积并与理论值比较,即可得出结论.
的体积并与理论值比较,即可得出结论.
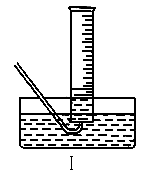
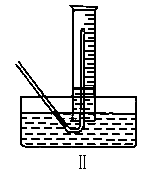
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的(忽略导管在量筒中所占的体积)________(填序号),理由是____________.
②若在标准状况下测量气体的体积,应选用的量筒的大小规格为________(选填“100mL”、“200mL”、“500mL”或“1000mL”).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com