
题目列表(包括答案和解析)
(10分)在10mL含有AlO2-离子的溶液中逐滴加入1mol/L的盐酸,所得Al(OH)3沉淀质量和所加盐酸的体积关系如图所示。
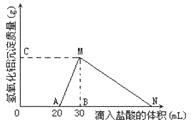
问:(1)此溶液中除含有AlO2- 外,还同时含有_ ___mol__ _ 离子;
(2)用离子方程式表示MN段发生的反应是
(3)原溶液中,c (AlO2-) 是 mol/L
(4)加盐酸到点N处,滴入的HCl溶液体积共为 ml
(10分)在一容积为2 L的密闭容器中,加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
(1)根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)为______________.
(2)该反应达到平衡时H2的转化率________.
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,达到新平衡时NH3的物质的量浓度不可能为____________.(填序号)
A、0.20 mol·L-1 b、0.12 mol·L-1 c、0.10 mol·L-1 d、0.08 mol·L-1
(4)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol·L-1),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线.
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时NH3的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(N2)、n(H2)、n(NH3)分别为a、b、c,则a、b、c之间应该满足的关系式为:
(6)若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1 K2(填“>” “=” 或 “<” )。
(10分)在有机反应中,反应物相同而条件不同,可得到不同的主产物,下式中R代表烃基,副产物均已略去。
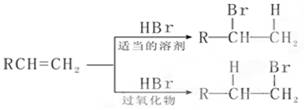
适当的溶剂(请注意H和Br所加成的位置)
请写出由CH3CH2CH2CH2Br分两步转变为CH3CH2CHBrCH3的反应的化学方程式,并注明反应类型
( )
( )
(10分)在密闭容器里,通入x mol H2(g)和y mol I2(g),发生反应H2(g)+I2(g) 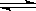 2HI(g)
△H<0。改变下列条件,反应速率将如何改变?(填“增大”“减小”或“不变”)
2HI(g)
△H<0。改变下列条件,反应速率将如何改变?(填“增大”“减小”或“不变”)
(1)升高温度 ;(2)加入催化剂 ;
(3)充入更多的H2 ;(4)扩大容器的体积 ;
(5)容器容积不变,通入氖气 。
(10分)在常温常压下,都用惰性材料作电极.分别电解(同浓度、同体积、通过相同电量)下列溶液:
A.CuSO4 B.AgNO3 C.KOH D.H2SO4 E.NaCl F.Na2SO4
通电一段时间切断电源,请填写下列空白。
(1)在A中一个电极上质量增加了0.128 g,在B中一个电极上质量增加 ,增加的物质是 .
(2) 在一极产生O2,同时另一极产生H2(填写序号,下同).
(3) 电解后,溶液中的C(OH-)增大
(4) 电解后,溶液的pH减小.
(5) 电解后,溶液的浓度增大而[H+]不变.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com