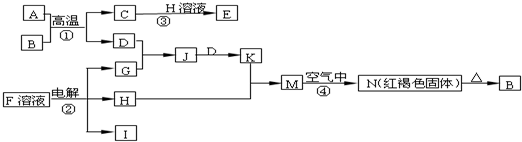
I、物质A-G有下图所示转化关系(部分反应物、生成物没有列出)其中A为某金属矿的主要成分,经过一系列反应可得到B和C.单质C可与E的浓溶液发生反应,G为砖红色沉淀.

请回答下列问题
(1)写出下列物质的化学式:B
SO2
SO2
E
H2SO4
H2SO4
G
Cu2O
Cu2O
(2)工业上B制备D在
接触室
接触室
设备中进行.
(3)反应②的化学方程式是
Cu+2H
2SO
4(浓)
CuSO
4+SO
2+2H
2O
Cu+2H
2SO
4(浓)
CuSO
4+SO
2+2H
2O
.
(4)将0.23molB和0.11mol氧气放入容积为1L的密闭容器中,发生反应①,在一定温度下,反应达到平衡,得到0.12molD,则反应的平衡常数K=
K=23.8
K=23.8
L?mol
-1,若温度不变,再加入0.50mol氧气后重新达到平衡,平衡
向右
向右
(填“向左”、“不变”、“向右”)移动,氧气的转化率
降低
降低
,(填“升高”“不变”或“降低”),D的体积分数
减小
减小
(填“增大”“不变”或“减小”)
II、“蓝瓶子”实验中使用的亚甲基蓝(C
16H
18ClN
3S?3H
2O)是一种氧化还原型指示剂,其氧化型呈蓝色,还原型呈无色:
氧化型(蓝色)+ne
-
还原型(无色)
将葡萄糖的碱性溶液放在锥形瓶中,滴加亚甲基蓝指示剂(蓝色),塞上瓶塞,溶液呈蓝色;静置一段时间,溶液褪色;振荡后,溶液又呈蓝色;再静置,又变无色;再振荡,又变蓝色…
(1)上述溶液由蓝色变无色的过程中,亚甲基蓝被
还原
还原
(填“氧化”或“还原”,下同),其中
还原
还原
剂是
葡萄糖
葡萄糖
(填物质名称).
(2)上述溶液由无色变蓝色的过程中,亚甲基蓝被
氧化
氧化
(填“氧化”或“还原”,下同),其中氧化剂是
氧气
氧气
(填物质名称).



 还原型(无色)
还原型(无色) Ⅰ.如下图所示,甲、乙之间的隔板K和活塞F都可左右自由移动,甲充入2molA和1molB,乙中充入2molC和1molHe,只有A为有色气体,此时K停在O处.在一定条件下发生逆反应:2A(g)+B(g)?2C(g)△H<0;反应达到平衡后,再恢复至原温度.回答下列问题:
Ⅰ.如下图所示,甲、乙之间的隔板K和活塞F都可左右自由移动,甲充入2molA和1molB,乙中充入2molC和1molHe,只有A为有色气体,此时K停在O处.在一定条件下发生逆反应:2A(g)+B(g)?2C(g)△H<0;反应达到平衡后,再恢复至原温度.回答下列问题: