
题目列表(包括答案和解析)
(7分)(1)今有A、B、C三种二甲苯;将它们分别进行一硝化反应,得到的产物分子式都是C8H9NO2,但A得到两种产物,B得到三种产物,C只得到一种产物。由此可以判断A、B、C各是下列哪一种结构,请将字母填入结构式后面的括号中。
(2)根据分子的相对分子质量M可以推测有机化合物的结构简式。若某种含C、H和卤素的化合物的M为48,写出其结构简式____________
(3)现有某种含C、H和卤素的化合物,测得两个M值,分别为64和66。分别写出它们的结构简式_____________________________________________________________
在推测有机化合物的结构时,可能用到的含量较多的同位素的质量数如下表:
| 元 素 | H | C | F | Cl | Br |
| 含量较多的同 位素的质量数 | 1 | 12 | 19 | 35,37 | 79,81 |
(7分)(1)今有A、B、C三种二甲苯;将它们分别进行一硝化反应,得到的产物分子式都是C8H9NO2,但A得到两种产物,B得到三种产物,C只得到一种产物。由此可以判断A、B、C各是下列哪一种结构,请将字母填入结构式后面的括号中。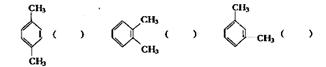
(2)根据分子的相对分子质量M可以推测有机化合物的结构简式。若某种含C、H和卤素的化合物的M为48,写出其结构简式____________
(3)现有某种含C、H和卤素的化合物,测得两个M值,分别为64和66。分别写出它们的结构简式_____________________________________________________________
在推测有机化合物的结构时,可能用到的含量较多的同位素的质量数如下表:
| 元 素 | H | C | F | Cl | Br |
| 含量较多的同 位素的质量数 | 1 | 12 | 19 | 35,37 | 79,81 |
(7分)(1)今有A、B、C三种二甲苯;将它们分别进行一硝化反应,得到的产物分子式都是C8H9NO2,但A得到两种产物,B得到三种产物,C只得到一种产物。由此可以判断A、B、C各是下列哪一种结构,请将字母填入结构式后面的括号中。
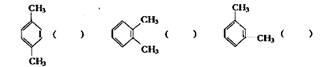
(2)根据分子的相对分子质量M可以推测有机化合物的结构简式。若某种含C、H和卤素的化合物的M为48,写出其结构简式____________
(3)现有某种含C、H和卤素的化合物,测得两个M值,分别为64和66。分别写出它们的结构简式_____________________________________________________________
在推测有机化合物的结构时,可能用到的含量较多的同位素的质量数如下表:
|
元 素 |
H |
C |
F |
Cl |
Br |
|
含量较多的同 位素的质量数 |
1 |
12 |
19 |
35,37 |
79,81 |
| 实验次数 | 称取样品的质量/g | 所加Ba(OH)2溶液的体积/L | 测得生成沉淀的质量/g |
| 1 | 0.858 | 0.5 | 1.379 |
| 2 | 1.716 | 0.5 | 2.758 2.758 |
| 3 | 2.574 | 0.5 | 4.137 |
| 4 | 3.432 | 0.5 | 5.516 |
| 5 | 4.290 | 0.5 | 5.516 |
| 6 | 5.148 | 0.5 | 5.516 |
| 1 |
| 100 |
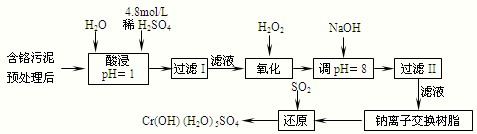
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 (>9溶解) |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com