
题目列表(包括答案和解析)
下列有关表述正确的是
A.H、D、T具有相同质子数,互为同素异形体
B.-OH 与![]() 组成元素相同,含有相同的电子数
组成元素相同,含有相同的电子数
C.CH2=CHC(CH3)3与氢气完全加成后,生成3,3-二甲基丁烷
D.结构示意图为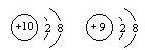 的两种粒子为同一种元素
的两种粒子为同一种元素
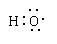 组成元素相同,含有相同的电子数
组成元素相同,含有相同的电子数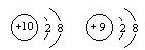 的两种粒子为同一种元素
的两种粒子为同一种元素下列有关表述正确的是
A.H、D、T具有相同质子数,互为同素异形体
B.-OH 与![]() 组成元素相同,含有相同的电子数
组成元素相同,含有相同的电子数
C.CH2=CHC(CH3)3与氢气完全加成后,生成3,3-二甲基丁烷
D.结构示意图为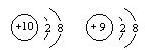 的两种粒子为同一种元素
的两种粒子为同一种元素
下列有关表述正确的是 ( )
A.H、D、T具有相同质子数,互为同素异形体
B.-OH 与![]() 组成元素相同,含有相同的电子数
组成元素相同,含有相同的电子数
C.CH2=CHC(CH3)3与氢气完全加成后,生成3,3-二甲基丁烷
D.结构示意图为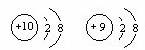 的两种粒子为同一种元素
的两种粒子为同一种元素
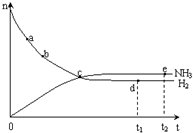 合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:
合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com