
题目列表(包括答案和解析)
 B.
B.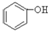 C.H2SO3
C.H2SO3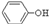 外、可能还含有OH-、S
外、可能还含有OH-、S| O | 2- 3 |
| O | - 3 |
 、S
、S| O | 2- 3 |
| O | - 3 |
| 实验步骤 | 预期现象和结论 | ||
| 步骤1:取少量待测液于试管中,加入足量的1mol?L-1BaCl2溶液,静置、过滤,得滤液和沉淀.将滤液分置于试管A、B中,沉淀置于试管C中. | |||
| 步骤2:往试管A中加入 |
| ||
| 步骤3:往试管B中加入 |
|||
| 步骤4:往试管C中加入2mol?L-1盐酸酸化,再滴入1~2滴品红溶液. |
|
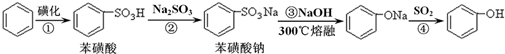
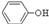
苯酚具有弱酸性,在空气中易被氧化。工业上以苯、硫酸、氢氧化钠、亚硫酸钠为原料合成苯酚的方法可简单表示为:

(1)根据上述反应判断下列三种物质的酸性由强到弱的顺序为 (填序号)。
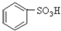
A. B.
B. C.H2SO3
C.H2SO3
(2)步骤④与使用CO2相比,使用SO2的优点是 (答一个方面)。
(3)经反应④得到的产物除 外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在
外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在 、SO32-、HSO3-,写出实验步骤、预期现象和结论。
、SO32-、HSO3-,写出实验步骤、预期现象和结论。
限选仪器及试剂:试管、滴管、玻璃棒、过滤装置和滤纸;2mol·L-1盐酸、1mol·L-1 BaCl2溶液、品红溶液、0.01 mol·L-1酸性KMnO4溶液、1 mol·L-1 FeCl3溶液、饱和溴水等。
|
实验步骤 |
预期现象和结论 |
|
步骤1:取少量待测液于试管中,加入足量的1 mol·L-1BaCl2溶液,静置、过滤,得滤液和沉淀。将滤液分置于试管A、B中,沉淀置于试管C中。 |
|
|
步骤2:往试管A中加入 。 |
,说明溶液中含有HSO3-。 |
|
步骤3:往试管B中加入 。 |
。 |
|
步骤4:往试管C中加入2 mol·L-1盐酸酸化,再滴入1~2滴品红溶液。 |
,说明溶液中含有SO32-。 |
(4)纯度测定:称取1.00g产品溶解于足量温水中,向其中加入足量饱和溴水(产品中除苯酚外,不含其它与饱和溴水反应生成沉淀的物质),苯酚全部生成三溴苯酚沉淀,经过滤、洗涤、干燥后,称得沉淀质量为3.31g,则产品中苯酚的质量分数为 。(苯酚的分子式为C6H6O,三溴苯酚的分子式为C6H3Br3O,它们的相对分子质量分别为94、331)
苯酚具有弱酸性,在空气中易被氧化。工业上以苯、硫酸、氢氧化钠、亚硫酸钠为原料合成苯酚的方法可简单表示为:
(1)根据上述反应判断下列三种物质的酸性由强到弱的顺序为 (填序号)。
A. B.
B. C.H2SO3
C.H2SO3
(2)步骤④与使用CO2相比,使用SO2的优点是 (答一个方面)。
(3)经反应④得到的产物除 外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在
外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在 、SO32-、HSO3-,写出实验步骤、预期现象和结论。
、SO32-、HSO3-,写出实验步骤、预期现象和结论。
限选仪器及试剂:试管、滴管、玻璃棒、过滤装置和滤纸;2mol·L-1盐酸、1mol·L-1 BaCl2溶液、品红溶液、0.01 mol·L-1酸性KMnO4溶液、1 mol·L-1 FeCl3溶液、饱和溴水等。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量待测液于试管中,加入足量的1 mol·L-1BaCl2溶液,静置、过滤,得滤液和沉淀。将滤液分置于试管A、B中,沉淀置于试管C中。 |  |
| 步骤2:往试管A中加入 。 | ,说明溶液中含有HSO3-。 |
| 步骤3:往试管B中加入 。 | 。 |
| 步骤4:往试管C中加入2 mol·L-1盐酸酸化,再滴入1~2滴品红溶液。 | ,说明溶液中含有SO32-。 |

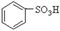 B.
B.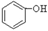 C.H2SO3
C.H2SO3 外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在
外、可能还含有OH-、SO32-、HSO3-等微粒。请设计实验方案,证明溶液中存在 、SO32-、HSO3-,写出实验步骤、预期现象和结论。
、SO32-、HSO3-,写出实验步骤、预期现象和结论。| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量待测液于试管中,加入足量的1 mol·L-1BaCl2溶液,静置、过滤,得滤液和沉淀。将滤液分置于试管A、B中,沉淀置于试管C中。 |  |
| 步骤2:往试管A中加入 。 | ,说明溶液中含有HSO3-。 |
| 步骤3:往试管B中加入 。 | 。 |
| 步骤4:往试管C中加入2 mol·L-1盐酸酸化,再滴入1~2滴品红溶液。 | ,说明溶液中含有SO32-。 |
某同学为了研究乙酸的性质,进行了如下实验:
(一)该同学利用下图所示的仪器和药品,设计了一个简单的一次性完成实验装置,来验证乙酸、碳酸和苯酚溶液酸性强弱.

(1)实验装置的连接顺序是:A→________→________→________→C→________→________→________→________→J
(2)写出实验中能说明碳酸比苯酚的酸性强的化学方程式________.
(二)为了研究乙酸的酯化反应,该同学进行了如下实验,步骤如下:在园底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品.请回答下列问题:
(1)反应中浓硫酸做________剂和吸水剂(或脱水剂).
(2)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加醋酸,边加热蒸馏.这样操作可以提高酯的产率,其原因是________.
(3)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图.若需要在图中圆括号内填入适当试剂,在方括号内填入适当分离方法.

下列试剂和分离方法正确的是________.
A.试剂a是氢氧化钠溶液,试剂b是稀硫酸;分离方法①是蒸馏,分离方法②是分液,分离方法③是蒸馏
B.试剂a是饱和碳酸钠溶液,试剂b是稀硫酸;分离方法①是分液,分离方法②是蒸馏,分离方法③是蒸馏
C.试剂a是饱和碳酸钠溶液,试剂b是稀硝酸;分离方法①是过滤,分离方法②是分液,分离方法③是蒸馏
D.试剂a是氢氧化钠溶液,试剂b是盐酸;分离方法①是分液,分离方法②是蒸馏,分离方法③是分液
(4)该同学在查阅资料时发现,乙酸和乙醇的酯化反应是分两步反应进行的,其反应的过程如下:
CH3COOH+HOC2H5 CH3COOC2H5+H2O
CH3COOC2H5+H2O
a.你认为其中属于加成反应的是________(填反应序号,在①②③④中选取)
b.在有机羧酸和醇的酯化反应中,脱水时,羧酸脱________基.为了探究酯化反应中的脱水方式,一般采取同位素示踪法,你认为用18O同位素进行标记时,下列标记正确的是________.
A.18O只能标记在醇羟基上
B.18O只能标记在羧酸的羟基上
C.18O可以标记在醇羟基上,也可以标记在羧酸的羟基上
D.18O可以标记在醇羟基上,也可以标记在羧酸的羟基上,还可以标记在羧酸的羰基上
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com