
题目列表(包括答案和解析)
(11分)某实验小组欲制取氧化铜并证明其能加快氯酸钾的分解,进行如下实验:
I.制取氧化铜
①称取2gCuSO4·5H2O研细后倒人烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液。直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是 (填实验序号),步骤①、③中研磨固体所用仪器的名称是 。
(2)步骤③中洗涤沉淀的操作是 。
Ⅱ.证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较。实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
| 实验序号 | KClO3质量 | 其他物质的质量 | 待测数据 |
| ④ | 1. 2g | 无其他物质 |
|
| ⑤ | 1. 2g | CuO 0.5g |
|
| ⑥ | 1. 2g | MnO2 0.5g |
|
回答下列问题:
(3)上述实验中的“待测数据”指 。
(4)若要证明实验中产生的气体是O2,可用小试管收集气体,后续操作为 。
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a. 。b. CuO的化学性质有没有改变。
(11分)某实验小组欲制取氧化铜并证明其能加快氯酸钾的分解,进行如下实验:
I.制取氧化铜
①称取2gCuSO4·5H2O研细后倒人烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH 溶液。直到不再产生沉淀,然后将所得混合物转
溶液。直到不再产生沉淀,然后将所得混合物转 移到蒸发皿,加热至沉淀全部变为黑色;
移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是 (填实验序号),步骤①、③中研磨固体所用仪器的名称是 。
(2)步骤③中洗涤沉淀的操作是 。
Ⅱ.证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较。实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
| 实验序号 | KClO3质量 | 其他物质的质量 | 待测数据 |
| ④ | 1. 2g 2g | 无其他物质 | |
| ⑤ | 1. 2g | Cu O 0.5g O 0.5g |  |
| ⑥ | 1. 2g | MnO2 0.5g | |
(11分)某实验小组欲制取氧化铜并证明其能加快氯酸钾的分解,进行如下实验:
I.制取氧化铜
①称取2gCuSO4·5H2O研细后倒人烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液。直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是 (填实验序号),步骤①、③中研磨固体所用仪器的名称是 。
(2)步骤③中洗涤沉淀的操作是 。
Ⅱ.证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较。实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
|
实验序号 |
KClO3质量 |
其他物质的质量 |
待测数据 |
|
④ |
1. 2g |
无其他物质 |
|
|
⑤ |
1. 2g |
CuO 0.5g |
|
|
⑥ |
1. 2g |
MnO2 0.5g |
|
回答下列问题:
(3)上述实验中的“待测数据”指 。
(4)若要证明实验中产生的气体是O2,可用小试管收集气体,后续操作为 。
(5)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a. 。b. CuO的化学性质有没有改变。
A.制取氧化铜
①称取2 g CuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
完成下列问题:
(1)上述实验步骤中需要使用玻璃棒的是_________(填实验序号),步骤①③中研磨固体所用仪器的名称是_______________。
(2)步骤③中洗涤沉淀的操作是_________________________________________________。
B.证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
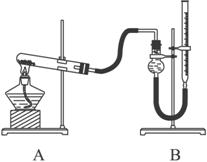
用下图装置进行实验,实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
④ | 1.2 g | 无其他物质 |
|
⑤ | 1.2 g | CuO 0.5 g |
|
⑥ | 1.2 g | MnO2 0.5 g |
|
完成下列问题:
(3)上述实验中的“待测数据”指_______________________。
(4)本实验装置图中量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是___________(填“酸式”或“碱式”)滴定管。
(5)若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,________________________________。
(6)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无须写出具体操作):
a.______________________________________________;b.CuO的化学性质没有改变。
某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)称取![]() 研细后倒入烧杯,加10mL蒸馏水溶解;
研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是__________(填实验序号),步骤①、③中研磨固体所用仪器的名称是_________________。
(2)步骤③中洗涤沉淀的操作是_______________________。
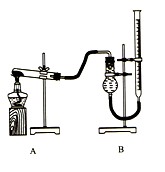
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较,用图示装置进行实验,实验时均以生成25 mL气体为准,其他可能影响实验的因素均已忽略,相关数据见下表:
| 实验序号 |
| 其他物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤ | 1.2g |
| |
| ⑥ | 1.2g |
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com