
题目列表(包括答案和解析)
高铁电池是一种新型可充电电池,其电池的总反应为:
3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH下列叙述不正确的是( )
A.放电时负极反应为:3Zn-6e-+6OH-=3Zn(OH)2
B.充电时阳极反应为:2Fe(OH)3+10OH6e=2FeO42-+8H2O
C.放电时每转移3mol电子,正极有1mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
高铁电池是一种新型可充电电池,其总反应为
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
下列有关叙述错误的是 ( )
A.放电时,每转移3mol电子有1molK2FeO4被氧化
B.放电时,正极附近溶液碱性增强
C.充电时,阴极反应为Zn(OH)2+2e-→Zn+2OH-
D.充电时,阴极附近溶液碱性减弱
“绿色奥运”是北京奥运会的主题之一。在北京奥运会上,具有我国自主知识产权的高铁电池电动环保汽车将大量使用。高铁电池是一种新型可充电电池,具有能长时间保持稳定的放电电压的优点。其总反应为: 3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
下列叙述中不正确的是( )
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-====FeO![]() +4H2O
+4H2O
C.放电时正极附近溶液的碱性增强
D.常温下,当500mLpH=13的电解质溶液升高一个单位时,电池中转移了电子1mol
(08淄博市模拟)“绿色奥运”是北京奥运会的主题之一。在北京奥运会上,具有我国自主知识产权的高铁电池电动环保汽车将大量使用。高铁电池是一种新型可充电电池,具有能长时间保持稳定的放电电压的优点。其总反应为:
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
下列叙述中不正确的是()
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-====FeO![]() +4H2O
+4H2O
C.放电时正极附近溶液的碱性增强
D.常温下,当500mLpH=13的电解质溶液升高一个单位时,电池中转移了电子1mol
| ||
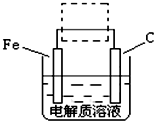 (FeSO4?7H2O)一起净水,其原理为
(FeSO4?7H2O)一起净水,其原理为 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH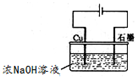 溶液的pH为
溶液的pH为湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com