

题目列表(包括答案和解析)
下列各单质及化合物之间的关系如下图,其中A为盐,C、M、N为日常生活中用途较广的金属单质,C是紫红色金属单质,常温下,可以用M或N制成的容器装运B的浓溶液,X具有磁性,B是工业上重要的化工原料。
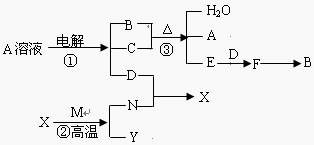
回答下列问题:
(1)N在周期表中的位置
(2)写出反应③的化学方程式
(3)写出反应①阳极的电极反应式 ,若阳极上析出的单质物质的量为0.01 mol,则阴极上析出的物质质量为 。
(4)工业生产中F→B反应是在 (填设备名称)中进行。
(5)写出反应②的化学方程式 ,若有16.8g的 N 生成,则转移的电子数为 。
如图表示各物质之间的转化关系。已知D、E、Z是中学化学常见的单质,其他都是化合物。Z、Y是氯碱工业的产品。D元素的原子最外层电子数与电子层数相等,且D的硫酸盐可作净水剂。E为日常生活中应用最广泛的金属。除反应①外,其他反应均在水溶液中进行。请回答下列问题。

(1)写出X的电子式:??????????? 。
(2)常温时pH =12的G溶液中,溶质的阳离子与溶质的阴离子浓度之差为?????????? (写出计算式)。
(3)在电镀工业中,若将E作为待镀金属,铜为镀层金属,则铜是____极,请写出在E电极上发生的电极反应式:????????????? 。
(4)写出反应③的离子方程式:??????????????????? 。
(5)现有无标签的Y和M的两种无色水溶液,不用其他任何试剂,请你设计一个简单的实验对这两种溶液加以鉴别???????????????? (回答实验操作、现象及结论)。
(6)A溶液与NaOH溶液混合可形成沉淀,某温度下此沉淀的Ksp =2.097×l0-39。将0.01 mol/L的A溶液与0.001 mol·L-1的NaOH溶液等体积混合,你认为能否形成沉淀____(填“能”或“不能”),请通过计算说明????????????????????????????? 。
如图表示各物质之间的转化关系。已知D、E、Z是中学化学常见的单质,其他都是化合物。Z、Y是氯碱工业的产品。D元素的原子最外层电子数与电子层数相等,且D的硫酸盐可作净水剂。E为日常生活中应用最广泛的金属。除反应①外,其他反应均在水溶液中进行。请回答下列问题。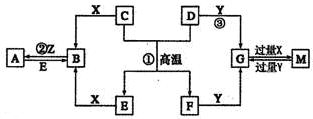
(1)写出X的电子式: 。
(2)常温时pH =12的G溶液中,溶质的阳离子与溶质的阴离子浓度之差为 (写出计算式)。
(3)在电镀工业中,若将E作为待镀金属,铜为镀层金属,则铜是____极,请写出在E电极上发生的电极反应式: 。
(4)写出反应③的离子方程式: 。
(5)现有无标签的Y和M的两种无色水溶液,不用其他任何试剂,请你设计一个简单的实验对这两种溶液加以鉴别 (回答实验操作、现象及结论)。
(6)A溶液与NaOH溶液混合可形成沉淀,某温度下此沉淀的Ksp =2.097×l0-39。将0.01 mol/L的A溶液与0.001 mol·L-1的NaOH溶液等体积混合,你认为能否形成沉淀____(填“能”或“不能”),请通过计算说明 。
已知a、b、I、K四种粒子都有10个电子,其结构特征如下:

A可作为工业上生产酸J的原料,B、C为非金属单质,E为红棕色固体,物质D由a、b构成,G是一种消毒剂的主要成分.各物质之间的转化关系如下图所示(个别产物略去).
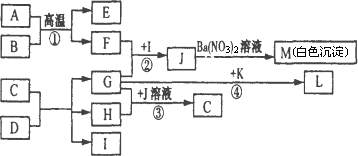
请回答下列问题:
(l)考虑到综合经济效益,工业生产K时,可采取的措施有________(填序号).a.使用催化剂 b.适当降低温度 c.适当增大压强 d.及时分离出产物 e.对原料进行循环利用 f.充分利用反应本身放出的热量 g.工厂地址选择在交通发达的大城市
(2)写出反应②的离子方程式:________________.
(3)反应④中,G(溶液)与K能以物质的量之比为1∶2反应生成L、H、I.L是一种火箭燃料,其分子中各原子均已达稳定结构.则L的电子式为________,该反应的化学方程式为________________.
(4)将F通入含等物质的量的D的溶液中,反应后的溶液能使甲基橙显红色,则此溶液中各微粒浓度的守恒关系是________________(只写一种).
(5)工业上反应①应在________(填设备名称)中进行.现有1 mol A参加反应,假设各步均反应完全,生成M的质量为1165 g,生成E的质量为320 g,则反应①的化学反应方程式为________________.
硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)已知:重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s)+4C(s)=BaS(s)+4CO(g)? △H= + 571.2 kJ?mol—1
BaS(s)= Ba(s)+S(s)? △H= +460 kJ?mol—1
已知:2C(s)+O2(g)=2CO(g)? △H= -221 kJ?mol—1
则:Ba(s)+S(s)+2O2(g)=BaSO4(s)? △H= ? ? 。
(2)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料。已知As2S3和HNO3有如下反应:
As2S3+10H++ 10NO3-=2H3AsO4+3S+10NO2↑+ 2H2O
当反应中转移电子的数目为2mol时,生成H3AsO4的物质的量为?? 。
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中主要含硫各物种(H2S、HS—、S2—)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如下图所示(忽略滴加过程H2S气体的逸出)。
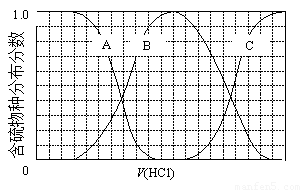
①含硫物种B表示???? 。在滴加盐酸过程中,溶液中c(Na+)与含硫各物种浓度的大小关系为 ? (填字母)。
a.c(Na+)= c(H2S)+c(HS—)+2c(S2—)
b.2c(Na+)=c(H2S)+c(HS—)+c(S2—)
c.c(Na+)=3[c(H2S)+c(HS—)+c(S2—)]
②NaHS溶液呈碱性,若向溶液中加入CuSO4溶液,恰好完全反应,所得溶液呈强酸性,其原因是 ? (用离子方程式表示)。
(4)硫的有机物(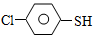 )与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O。
)与甲醛、氯化氢以物质的量之比1:1:1反应,可获得一种杀虫剂中间体X和H2O。
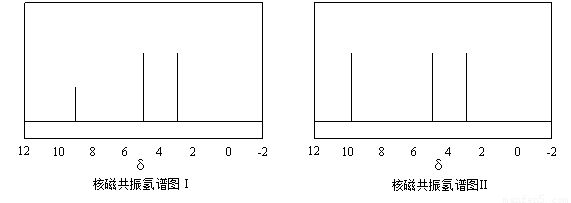
 及X的核磁共振氢谱如下图,其中???? (填“Ⅰ”或“Ⅱ”)为
及X的核磁共振氢谱如下图,其中???? (填“Ⅰ”或“Ⅱ”)为 的核磁共振氢谱图。写出X的结构简式:???? 。
的核磁共振氢谱图。写出X的结构简式:???? 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com