
题目列表(包括答案和解析)
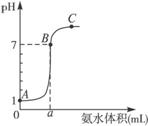
A.盐酸的浓度为1 mol/L
B.在B点:c(![]() )=c(Cl-)>c(OH-)=c(H+),且a>10
)=c(Cl-)>c(OH-)=c(H+),且a>10
C.在A、B间任意一点:c(Cl-)>c(![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.在C点:c(![]() )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)
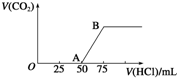 向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )
向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )A、OA段所发生反应的离子方程式:H++OH-═H2O;CO32-+H+═HCO
| ||
| B、NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1:1 | ||
| C、产生的CO2体积(标准状况下)为0.056 L | ||
| D、原NaOH溶液的物质的量浓度为0.5 mol?L-1 |
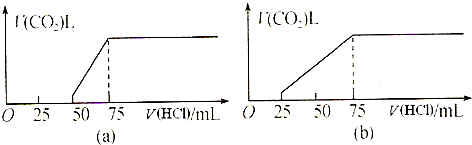
有50mL NaOH溶液,向其中逐渐通入一定量的CO2,取此溶液10mL将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L―1的HCl溶液,产生CO2气体的体积(标准状况)与所加入盐酸体积之间的关系如图所示:
回答下列问题:
(1)稀释后的溶液中含有的溶质为 。
(2)标准状况下生成CO2的体积为 。
(3)原NaOH溶液的物质的量浓度为 。
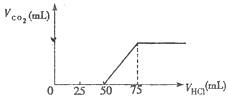
向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )

A.OA段所发生反应的离子方程式: H++OH-=H2O;CO32-+H+=HCO3-
B.NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1∶1。
C.产生的CO2体积(标准状况下)为0.056 L
D.原NaOH溶液的物质的量浓度为0.5 mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com