
题目列表(包括答案和解析)
甲、乙、丙、丁是原子序数依次增大的四种短周期元素,A、B、C、D、E是由其中的两种或三种元素组成的化合物,F是由丙元素形成的单质。已知:A + B = D + F,A + C = E + F; 0.1 mol·L-1D溶液的pH为13(25℃)。下列说法正确的是(??? )
A.原子半径:丁>丙>乙>甲
B.1 molA与足量B完全反应共转移了2 mol电子
C.丙元素在周期表中的位置为第二周期第ⅣA族
D.A中既有离子键又有共价键
甲、乙、丙、丁是原子序数依次增大的四种短周期元素,A、B、C、D、E是由其中的两种或三种元素组成的化合物,F是由丙元素形成的单质。已知:A + B =" D" + F,A + C =" E" + F; 0.1 mol·L-1D溶液的pH为13(25℃)。下列说法正确的是( )
A.原子半径:丁>丙>乙>甲
B.1 molA与足量B完全反应共转移了2 mol电子
C.丙元素在周期表中的位置为第二周期第ⅣA族
D.A中既有离子键又有共价键
甲、乙、丙、戊都具有如图所示的结构或结构单元,图中正四面体以外可能有的部分未画出,细(虚)线不表示化学键或分子间作用力,X与Y可以相同也可以不同。已知甲、乙是同类晶体中的各自结构单元,单质甲能与乙发生置换反应,丙、丁、戊三种粒子含有等量的电子数,其中丙与丁晶体类型相同,常温下化合物丁呈液态,戊是阳离子。
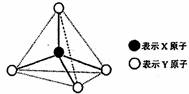
(1)丁的电子式是 ,丁固态时的晶体类型为 。
(2)常温下戊的硝酸盐溶液的pH 。
A.>7 B.=7 C.<7 D.以上都有可能
(3)甲与乙发生置换反应的化学方程式为 。
(4)丙分子的结构式是 ,它是目前重要的能源物质,现代高能电池中常用丙作燃料电池的原料,在碱性介质(KOH溶液)情况下,其负极反应的电极方程式为 。
 2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热
2DB3,若3.2gDB2完全转化为DB3气体时放热akJ;1mol DB3气体完全转化为其水化物放热bkJ,则标况下33.6L DB2完全完成上述两步反应放热湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com