
题目列表(包括答案和解析)
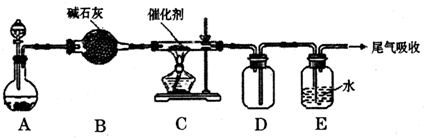
(08哈师大附中三模)某化学活动小组为了模拟工业合成氨的生产流程,设计了如下实验装置:

(1) 写出工业合成氨的化学方程式: ;
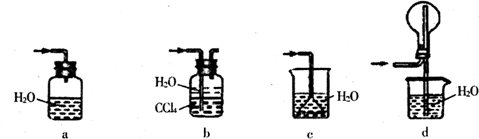
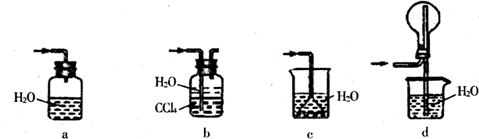
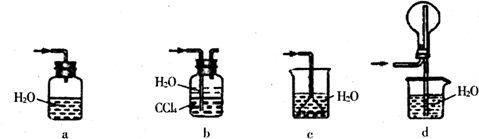
(2) 从下图中选择E中的合适装置 (填写相应的序号);

(3) 写出C中反应的离子方程式 ;
(4) 装置D的作用除了将气体混合外,还有 、 ;
(5)可用装置C来吸收氨是因为氨在水中溶解度大,并且 ;
(6) 若G中盛有500mL水,吸收的氨的体积换算成标准状况为VmL,则G中所得溶液的质量分数可表示为 。
(08赤峰二中模拟)(15分)已知:NH4Cl 溶液和NaNO2固体反应可以制备N2,其原理为:

某化学兴趣小组为了模拟N2和H2合成NH3实验进行了相关操作。
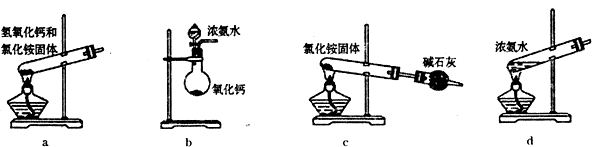
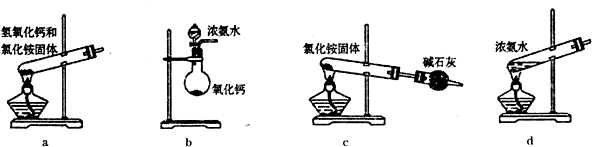
⑴NH4Cl 溶液和NaNO2反应制备N2 所用的发生装置是

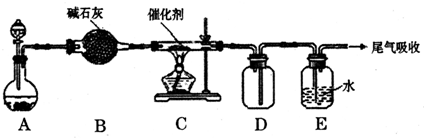
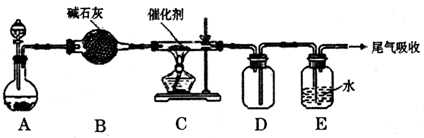
⑵该活动小组用下图中的装置及所给药品(图中夹持仪器已略去)来探究工业上N2和H2合成NH3的反应。

请回答下列问题:
①检查完装置的气密性、加入药品后,排除装置内的空气后开始进行实验,此时首先应进行的操作是 其目的是
②实验测得C中酚酞变色所用时间与V(N2)/V(H2)的关系如下表:
| 第一组 | 第二组 | 第三组 | 第四组 | 第五组 |
V(N2)/V(H2) | 1:1 | 1:3 | 1:6 | 3:1 | 5:1 |
时间(min) | 6~7 | 3~4 | 9~10 | 7~8 | 8~9 |
模拟合成氨气实验中V(N2)/V(H2)最佳值为 ,实验中调节该体积比的方法是
③工业上常采取 方法提高H2的转化率、降低成本。
① 用此装置合成NH3时,反应物的转化率一般<50%。有的同学认为用C装置吸收产物会产生倒吸,你认为合理吗?说明理由。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com