
题目列表(包括答案和解析)
现有aA、bB、cC、dD、eE、fF六种短周期元素,原子序数依次增大,A、B、C、D都是生命不可缺少的重要元素。已知它们原子序数存在如下关系:a+b=c, a+c=d, b+c=f;元素A、B、C和D都能形成原子个数比为1:1和1:2的化合物;元素E的原子是短周期主族元素中原子半径最大的原子。其中由A、B、D三元素组成的化合物甲,其化学式灾BA4D;由D、E两元素形成原子个数比为1:1化合物乙;C的气态氢化物和最高价氧化物的水化物分别为丙和丁。请根据要求回答下列问题:
(1)经测定,A2D2的水溶液呈弱酸性。请写出第一步的电离方程式 。
(2)用甲和单质D2可设计成燃料电池,若电解质溶液为浓KOH溶液,则正极的电极反应式为 。
(3)3.9g乙与足量的水反应,电子转移的物质的量是 。
(4)单质F与E的最高价氧化物的水化物的溶液反应的离子方程式是 。
(5)常温下向25mL 0.1mol?L―1丙溶液中逐滴滴加0.1mol?L―1丁溶液,滴加过程中混合溶液pH的变化曲线如下图所示:

①图中m点由水电离也的OH―的物质的量浓度为 ;
②p点时,丙溶液和丁溶液恰好完全反应,则p点溶液中各备种离子浓度由大到小的顺序为 。
(12分) 现有下列十种物质:
①H2 ②铝 ③CaO ④CO2 ⑤H2SO4 ⑥Ba(OH)2
⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 | | | | | |
(12分) 现有下列十种物质:
①H2 ②铝 ③CaO ④CO2 ⑤H2SO4 ⑥Ba(OH)2
⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
|
分类标准 |
金属单质 |
氧化物 |
溶液 |
胶体 |
电解质 |
|
属于该类的物质 |
|
|
|
|
|
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-= H2O,该离子反应对应的化学方程式为__________________________________________________________。
(3)⑩在水中的电离方程式为__________________________________________________,
(4)少量的④通入⑥的溶液中反应的离子方程式为________________________________。
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是____________(填化学式),氧化剂与还原剂的物质的量之比是_____________,当有5.4g Al发生反应时,转移电子的物质的量为_________________。该反应的离子方程式为______________________________。
(12分)反应aA(g)+bB(g) cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
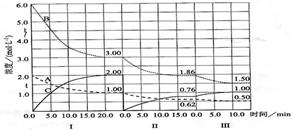
回答问题:
(1)反应的化学方程式中,a:b:c为 ;
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为 ;
(3) B的平衡转化率aI(B)、aII(B)、aIII(B)中最小的是 ,其值是 ;
(4)由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是 ;
(5)比较第II阶段反应温度(T1)和第III阶段反应速度(T3)的高低:T2 T3
填“>、=、<”判断的理由是 ;
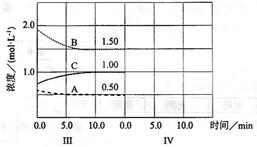
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).
(10分)现有aA、bB、cC、dD、eE五种短周期元素,它们都是生命体不可缺少的重要元素已知它们的原子序数有如下关系:a+b=c,a+c=d,c+d=e,B、D、E都有多种同素异形体。B的化合物种类与A的化合物种类何者更多,目前学术界还有争议,但有一点是肯定的,那就是没有第三种元素的化合物种数会超出它们。根据以上信息回答下列有关问题:
(1)请比较B2A4、C2A4、E2A4三种化合物的沸点由高到低的顺序 。
(2)从给定的元素中选出若干种组成化合物,写出相对分子质量最小的离子化合物的化学式 ;
(3)从题中元素为选择对象,写出不少于三种炸药的化学式或名称。 、 、 。
 (4)有人设想某种分子式为C4N4O8的物质(该物质中同种原子的化学环境完全相同)是一种威力极强的炸药,请推测它的结构简式。
(4)有人设想某种分子式为C4N4O8的物质(该物质中同种原子的化学环境完全相同)是一种威力极强的炸药,请推测它的结构简式。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com