
题目列表(包括答案和解析)
CH4(g)+H2O(g)![]() CO(g)+3H2(g);ΔH>0
CO(g)+3H2(g);ΔH>0
请根据题目要求回答下列问题。
(1)在一定条件下,将0.05molCH4和0.10molH2O气放入容积
(2)在其他条件不变的情况下降低温度,则逆反应速率__________(填“增大”“减小”或“不变”,下同);在其他条件不变的情况下加压,则正反应速率____________________。
(3)在一定条件下,当该反应处于化学平衡状态时,下列操作可使化学平衡向正反应方向移动的是__________(填序号)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 F.移出水蒸气
(4)在一定温度下,将1.0 mol CH4和2.0molH2O(g)通入某一恒压容器中,达到化学平衡时,混合气共4.0mol,则CH4的转化率为___________;若其他条件不变,起始时加入amol CH4、bmol H2O(g)、cmolCO和dmolH2,达到平衡时,各组分体积分数与上述平衡完全相等,则a、b和c满足的关系为___________(用字母表示)。
| |||||||||||||||||||||||||||||||

| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
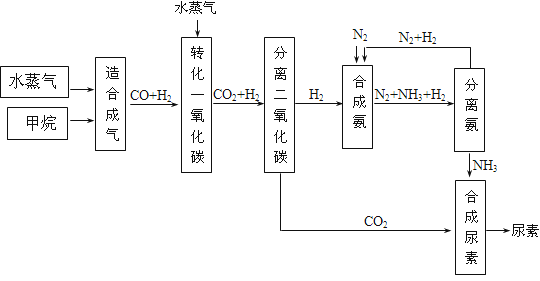
四川有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):
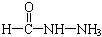
请填写下列空白:
(1)已知0.5 mol甲烷与0.5 mol水蒸汽在t ℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,该反应的热化学方程式是: 。
(2)在合成氨的实际生产过程中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气,请运用化学反应速率和化学平衡的观点说明采取该措施的理由: 。
(3)当甲烷合成氨气的转化率为75%时,以5.60×107 L甲烷为原料能够合成: L氨气。(假设体积均在标准状况下测定)
(4)已知尿素的结构简式为![]() 请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
① ;② 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com