
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
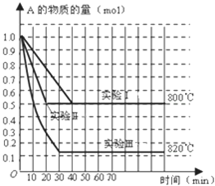 ‘⁄“ª√б’»ð∆˜÷–∑¢…˙ªØ—ß∑¥”¶£∫2A£®g£©?B£®g£©+C£®g£©£ª‘⁄º∏÷÷≤ªÕ¨Ãıº˛œ¬Ω¯––£¨∆‰÷–B°¢Cµƒ∆ ºŒÔ÷ µƒ¡øŒ™0£¨∑¥”¶ŒÔAµƒŒÔ÷ µƒ¡øÀÊ ±º‰±‰ªØ»ÁÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «£®°°°°£©
‘⁄“ª√б’»ð∆˜÷–∑¢…˙ªØ—ß∑¥”¶£∫2A£®g£©?B£®g£©+C£®g£©£ª‘⁄º∏÷÷≤ªÕ¨Ãıº˛œ¬Ω¯––£¨∆‰÷–B°¢Cµƒ∆ ºŒÔ÷ µƒ¡øŒ™0£¨∑¥”¶ŒÔAµƒŒÔ÷ µƒ¡øÀÊ ±º‰±‰ªØ»ÁÕºÀ˘ 棨œ¬¡–Àµ∑®’˝»∑µƒ «£®°°°°£©| A°¢∏√∑¥”¶’˝∑¥”¶Œ™∑≈»»∑¥”¶ | B°¢ µ—È¢Ú∫Õ µ—È¢Ò±»Ωœ£¨ µ—È¢Ú“ª∂® π”√¡À¥þªØº¡ | C°¢‘⁄ µ—È¢Ò÷–£¨»Ù»ð∆˜µƒÃª˝Œ™0.5L£¨‘Ú¥”ø™ ºµΩ¥Ô∆Ω∫‚ ±º‰ƒ⁄Bµƒ∆Ωæ˘∑¥”¶ÀŸ¬ Œ™0.025mol/£®L?min£© | D°¢‘⁄800°Ê ±£¨‘ˆ¥Û—π«ø£¨»Ù∑¥”¶÷ÿ–¬¥Ô∆Ω∫‚ ±ªÏ∫œ∆¯ÃÂ∂‘«‚∆¯µƒœý∂‘√Ð∂»Œ™64.5£¨‘ÚAµƒœý∂‘∑÷◊”÷ ¡øŒ™129 |
(1)»ÙΩ´4 mol A∫Õ2 mol B‘⁄
(2)»Ù∞—a mol A∫Õb mol B≥‰»Î“ª√б’»ð∆˜÷–£¨¥ÔµΩ∆Ω∫‚ ±À¸√«µƒŒÔ÷ µƒ¡ø¬˙◊„£∫
n(A)£´n(B)=n(C)£¨‘ÚAµƒ◊™ªØ¬ Œ™____________°£
(3)»ÙΩ´4 mol A∫Õ2 mol Bº”»Îê˝ø…±‰µƒµ»—π»ð∆˜÷–£¨“ª∂®Œ¬∂»œ¬¥ÔµΩ∆Ω∫‚◊¥Ã¨£¨≤‚µ√∆¯ÃÂ◊ÐŒÔ÷ µƒ¡øŒ™4.2 mol°£¥À ±£¨ªÏ∫œ∆¯ÃÂ÷–CµƒÃª˝∑÷ ˝Œ™____________£ª»Ù‘ŸÕ®»Î…Ÿ¡øB∆¯Ã£¨ÃÂœµ÷–AµƒÃª˝∑÷ ˝____________(ÃÓ°∞‘ˆ¥Û°±°∞ºı–°°±ªÚ°∞≤ª±‰°±)£¨»Ù“™ πAµƒÃª˝∑÷ ˝‘Ÿ¥ÔµΩ”Α≠∆Ω∫‚◊¥Ã¨œýÕ¨£¨ø…≤…»°µƒ¥Î ©”–________________________°£
(4)œ¬Õº «“ª∂®Ãıº˛œ¬∏√∑¥”¶π˝≥Ã÷–£¨ÃÂœµƒ⁄∏˜ŒÔ÷ ≈®∂»µƒ±‰ªØ«Èøˆ°£∑¥”¶¥¶”⁄∆Ω∫‚◊¥Ã¨µƒ ±º‰ «________£¨t2 ±«˙œþ∑¢…˙±‰ªØµƒ‘≠“Ú «_________________£¨»Ù‘⁄t4 ±Ω´Bµƒ≈®∂»‘ˆ¥Û0.1 mol°§L-1£¨«Î‘⁄œ¬Õº÷–ª≠≥ˆ∏˜ŒÔ÷ ≈®∂»µƒ±‰ªØ«Èøˆ°£

 ”–»Áœ¬ªØ—ß∑¥”¶£∫2A£®g£©+B£®g£©?2C£®g£©£¨°˜H£º0£Æ
”–»Áœ¬ªØ—ß∑¥”¶£∫2A£®g£©+B£®g£©?2C£®g£©£¨°˜H£º0£ÆœÚ2L√б’»ð∆˜÷–Õ®»Îamol ∆¯Ã A∫Õbmol∆¯ÃÂB£¨‘⁄“ª∂®Ãıº˛œ¬∑¢…˙∑¥”¶£∫
xA(g)+ yB(g) pC(g) + qD(g)°£“—÷™£∫∆Ωæ˘∑¥”¶ÀŸ¬ V(C) =1/2V(A) £ª∑¥”¶2min ±£¨Aµƒ≈®∂»ºı…Ÿ¡À1/3 £¨BµƒŒÔ÷ µƒ¡øºı…Ÿ¡Àa/2 mol£¨”–a mol D…˙≥…°£ªÿ¥œ¬¡–Œ £∫
pC(g) + qD(g)°£“—÷™£∫∆Ωæ˘∑¥”¶ÀŸ¬ V(C) =1/2V(A) £ª∑¥”¶2min ±£¨Aµƒ≈®∂»ºı…Ÿ¡À1/3 £¨BµƒŒÔ÷ µƒ¡øºı…Ÿ¡Àa/2 mol£¨”–a mol D…˙≥…°£ªÿ¥œ¬¡–Œ £∫
£®1£©∑¥”¶2minƒ⁄£¨Aµƒ∆Ωæ˘∑¥”¶ÀŸ¬ « mol?L-1?min-1£ª
£®2£©‘≠ªØ—ß∑Ω≥à Ω÷–£¨ªØ—ߺ∆¡ø ˝ «£∫
A(g)+ B(g)  C(g) + D(g)
C(g) + D(g)
£®3£©∑¥”¶∆Ω∫‚ ±£¨DŒ™2a mol£¨‘ÚBµƒ◊™ªØ¬ Œ™ £ª
£®4£©»Áπ˚÷ª…˝∏þ∑¥”¶Œ¬∂»£¨∆‰À˚∑¥”¶Ãıº˛≤ª±‰£¨∆Ω∫‚ ±DŒ™ 1.5a mol£¨‘Ú∏√∑¥”¶
µƒ°˜H 0£ª£®ÃÓ°∞£æ°±°¢°∞£º°±ªÚ°∞£Ω°±£©
£®5£©»Áπ˚∆‰À˚Ãıº˛≤ª±‰£¨Ω´»ð∆˜µƒ»ðª˝±‰Œ™1L£¨Ω¯––Õ¨—˘µƒ µ—È£¨‘ڔ΅œ ˆ∑¥”¶±»Ωœ£∫
¢Ÿ∑¥”¶ÀŸ¬ ‘ˆ¥Û £¨¿Ì”… «Ãª˝ºı–°£¨∑¥”¶ŒÔµƒ≈®∂»‘ˆ¥Û£¨“Ú∂¯ π∑¥”¶ÀŸ¬ ‘ˆ¥Û£ª
¢⁄∆Ω∫‚ ±∑¥”¶ŒÔµƒ◊™ªØ¬ £®ÃÓ°∞‘ˆ¥Û°±°¢°∞ºı–°°±ªÚ°∞≤ª±‰°±£©£¨¿Ì”… «
œÚ2L√б’»ð∆˜÷–Õ®»Îamol ∆¯Ã A∫Õbmol∆¯ÃÂB£¨‘⁄“ª∂®Ãıº˛œ¬∑¢…˙∑¥”¶£∫
xA(g)+ yB(g) pC(g) + qD(g)°£“—÷™£∫∆Ωæ˘∑¥”¶ÀŸ¬ V(C) =1/2V(A) £ª∑¥”¶2min ±£¨Aµƒ≈®∂»ºı…Ÿ¡À1/3 £¨BµƒŒÔ÷ µƒ¡øºı…Ÿ¡Àa/2 mol£¨”–a mol D…˙≥…°£ªÿ¥œ¬¡–Œ £∫
pC(g) + qD(g)°£“—÷™£∫∆Ωæ˘∑¥”¶ÀŸ¬ V(C) =1/2V(A) £ª∑¥”¶2min ±£¨Aµƒ≈®∂»ºı…Ÿ¡À1/3 £¨BµƒŒÔ÷ µƒ¡øºı…Ÿ¡Àa/2 mol£¨”–a mol D…˙≥…°£ªÿ¥œ¬¡–Œ £∫
£®1£©∑¥”¶2minƒ⁄£¨Aµƒ∆Ωæ˘∑¥”¶ÀŸ¬ « mol?L-1?min-1£ª
£®2£©‘≠ªØ—ß∑Ω≥à Ω÷–£¨ªØ—ߺ∆¡ø ˝ «£∫
A(g)+ B(g)  C(g) + D(g)
C(g) + D(g)
£®3£©∑¥”¶∆Ω∫‚ ±£¨DŒ™2a mol£¨‘ÚBµƒ◊™ªØ¬ Œ™ £ª
£®4£©»Áπ˚÷ª…˝∏þ∑¥”¶Œ¬∂»£¨∆‰À˚∑¥”¶Ãıº˛≤ª±‰£¨∆Ω∫‚ ±DŒ™ 1.5a mol£¨‘Ú∏√∑¥”¶
µƒ°˜H 0£ª£®ÃÓ°∞£æ°±°¢°∞£º°±ªÚ°∞£Ω°±£©
£®5£©»Áπ˚∆‰À˚Ãıº˛≤ª±‰£¨Ω´»ð∆˜µƒ»ðª˝±‰Œ™1L£¨Ω¯––Õ¨—˘µƒ µ—È£¨‘ڔ΅œ ˆ∑¥”¶±»Ωœ£∫
¢Ÿ∑¥”¶ÀŸ¬ ‘ˆ¥Û £¨¿Ì”… «Ãª˝ºı–°£¨∑¥”¶ŒÔµƒ≈®∂»‘ˆ¥Û£¨“Ú∂¯ π∑¥”¶ÀŸ¬ ‘ˆ¥Û£ª
¢⁄∆Ω∫‚ ±∑¥”¶ŒÔµƒ◊™ªØ¬ £®ÃÓ°∞‘ˆ¥Û°±°¢°∞ºı–°°±ªÚ°∞≤ª±‰°±£©£¨¿Ì”… «
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com