有关元素A、B、C、D的信息如下:
| 元 素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 地壳中含量最高的元素,A与B可形成一种质量比为 7:12的化合物(丙) |
| C | 单质曾用于焊接钢轨 |
| D | 单质是生活中常见金属,其制品在自然环境中被腐蚀呈现红棕色 |
请回答下列问题:
(1)用C单质来焊接钢轨的化学方程式是______.
(2)有关C与D元素,下列说法正确的是______(填序号).
①C或D的高价盐均可用做净水剂
②用C或D单质做成的槽车,都可用来运输甲的稀溶液
③C、D的单质与稀硫酸组成的原电池,C电极发生氧化反应
④C的合金可用来做车船材料和门窗等
(3)B的一种氢化物在碱性溶液中可与丙反应,生成物中A元素只显其最高价态,该反应的离子方程式是______.
(4)现取1mol/L 100mL的C的氯化物溶液,向其中加入1mol/L氢氧化钠溶液产生了3.9g的沉淀,则加入的氢氧化钠溶液体积可能是______mL.
(5)已知:2AB
2(g)

A
2B
4(g);△H<0.在恒温恒容条件下,将一定量AB
2和A
2B
4的混合气体通入容积为2L的密闭

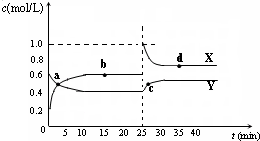
容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
①a、b、c、d四个点中,化学反应处于平衡状态的是______ 点.
②25min时,增加了______(填物质的化学式)______mol.
③a、b、c、d四个点中所表示的反应体系中,气体颜色由深到浅的顺序是______ (填字母).

 、Cl一四种离子,且c(
、Cl一四种离子,且c( )>c(Cl-)>c(OH-)>c(H+),则这两种溶质是 .
)>c(Cl-)>c(OH-)>c(H+),则这两种溶质是 .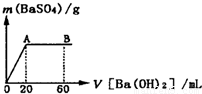
 (2011?郑州二模)利用所学化学反应原理,解决以下问题:
(2011?郑州二模)利用所学化学反应原理,解决以下问题: NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+ A2B4(g);△H<0.在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭
A2B4(g);△H<0.在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭 容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
 容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.