
题目列表(包括答案和解析)
①向硫酸铜溶液中加入适量铁粉
②等物质的量浓度、等体积的硫酸铵和氯化钡溶液
③等物质的量的碳酸氢钠与过氧化钠固体
④在溴化钠溶液中通入过量氯气
A.①② B.③④ C.①③ D.②④
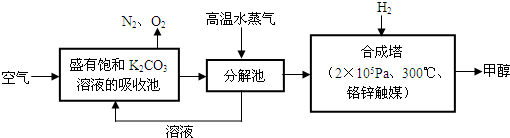
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
(1)在煤的气化反应器中发生如下几种反应:
C(s)十H2O(g)=CO(g)+H2(g) ΔH=+131 kJ/mol
C(s)+O2(g)=CO2(g) ΔH=-394 kJ/mol
CO(g)+![]() O2(g)=CO2(g) ΔH=-283 kJ/mol
O2(g)=CO2(g) ΔH=-283 kJ/mol
则CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH=________
H2(g)+CO2(g) ΔH=________
(2)已知830℃时,在一个容积固定的密闭容器中,发生反应
CO(g)+H2O(g)![]() H2(g)+CO2(g)下列能判断该反应达到化学平衡状态的是________(填字母).
H2(g)+CO2(g)下列能判断该反应达到化学平衡状态的是________(填字母).
a.容器中的压强不变
b.1 mol H-H键断裂的同时断裂2 mol H-O键
c.v正(CO)=v逆(H2O)
d.c(CO)=c(H2)
又知此温度下该反应的平衡常数K=1,等物质的量的CO和H2O反应达到平衡时,CO的转化率为________.
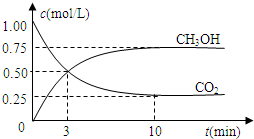
(3)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)![]() H2(g)+CO2(g),得到如下三组数据:
H2(g)+CO2(g),得到如下三组数据:

①实验1中以v(CO2)表示的反应速率为________.
②该反应的逆反应为________(填“吸”或“放’’)热反应
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3 min,则a、b应满足的关系是________(用含a、b的数学式表示).
(4)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:3H2(g)+CO2(g)![]() CH3OH(g)+H2O(g),下图表示
CH3OH(g)+H2O(g),下图表示

该反应进行过程中能量(单位为kJ·mol)的变化.
①在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,下列措施中能使c(CH3OH)增大的是________(填字母)
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1 mol CO2和3 mol H2
②当反应达到平衡时不断改变条件(但不改变各组分物质的量和状态且只改变一个条件)反应速率随时间的变化如下图:其中表示平衡混合物中CH3OH含量最高的一段时间是________;如t0~t1平衡常数为K1,t2~t3平衡常数为K2,则K1________K2(填“大于”、“等于”或“小于”).

(5)煤气化过程中会生成少量CH4,已知CH4与CaSO4反应生成CaS、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为________.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。(1) 在煤的气化反应器中发生如下几种反应:
C(s)十H2O(g)=CO(g)+H2(g) △H= +131kJ/mol
C(s)+O2(g)=CO2(g) △H= —394kJ/mol
CO(g)+ O2(g)=CO2(g) △H= —283kJ/mol
O2(g)=CO2(g) △H= —283kJ/mol
则CO(g)+H2O(g) H2(g)+CO2(g)△H=
H2(g)+CO2(g)△H=
(2)已知830℃时,在一个容积固定的密闭容器中,发生反应
CO(g)+H2O(g) H2(g)+CO2(g)下列能判断该反应达到化学平衡状态的是 (填字母)。
H2(g)+CO2(g)下列能判断该反应达到化学平衡状态的是 (填字母)。
a.容器中的压强不变 b.1 mol H-H键断裂的同时断裂2 mol H-O键
c.  (CO)=
(CO)= (H2O) d.c(CO)=c(H2)
(H2O) d.c(CO)=c(H2)
又知此温度下该反应的平衡常数K=1,等物质的量的CO和H2O反应达到平衡时,CO的转化率为 .
(3) 将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应
CO(g)+H2O(g) H2(g)+CO2(g),得到如下三组数据:
H2(g)+CO2(g),得到如下三组数据:
①实验l中以 (CO2)表示的反应速率为 。
(CO2)表示的反应速率为 。
②该反应的逆反应为 (填“吸”或“放’’)热反应
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3min,则a、b应满足的关系是 (用含a、b的数学式表示)。
(4)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:
3H2(g)+CO2(g) CH3OH(g)+H2O(g),右图表示
CH3OH(g)+H2O(g),右图表示
该反应进行过程中能量(单位为kJ·mol)的变化。
①在体积为1 L的恒容密闭容器中,充入l molCO2和3molH2,下列措施中能使c(CH3OH)增大的是 (填字母)
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来 d.再充入l mol CO2和3 molH2
②当反应达到平衡时不断改变条件(但不改变
各组分物质的量和状态且只改变一个条件)反应速率随时间的变化如右图:其中表示平衡混合物中CH3OH含量最高的一段时间是 ;如t0~t1平衡常数为K1,t2~t3平衡常数为K2,则K1 K2(填“大于”、“等于”或“小于”)。
(5)煤气化过程中会生成少量CH4,已知CH4与CaSO4反应生成CaS、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为 。
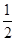 O2(g)=CO2(g) △H= —283kJ/mol
O2(g)=CO2(g) △H= —283kJ/mol H2(g)+CO2(g)△H=
H2(g)+CO2(g)△H=  H2(g)+CO2(g)下列能判断该反应达到化学平衡状态的是 (填字母)。
H2(g)+CO2(g)下列能判断该反应达到化学平衡状态的是 (填字母)。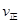 (CO)=
(CO)=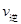 (H2O) d.c(CO)=c(H2)
(H2O) d.c(CO)=c(H2)  H2(g)+CO2(g),得到如下三组数据:
H2(g)+CO2(g),得到如下三组数据:
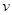 (CO2)表示的反应速率为 。
(CO2)表示的反应速率为 。 CH3OH(g)+H2O(g),右图表示
CH3OH(g)+H2O(g),右图表示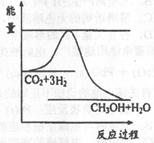

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com