
题目列表(包括答案和解析)

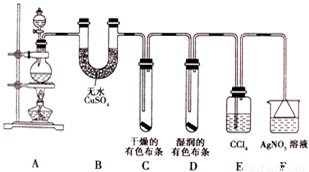
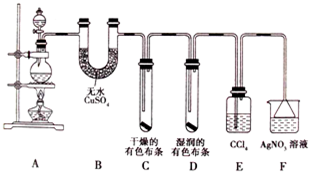

某校化学实验兴趣小组进行实验室制取氯气,并验证氯气的某些化学性质实验,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)下列方法中,可制得氯气的正确组合是 。
① MnO2和浓盐酸混合共热;② NaCl固体和浓硫酸混合共热;
③ 次氯酸钠和稀盐酸混合; ④ K2Cr2O7和浓盐酸混合;
⑤ KClO3和浓盐酸混合; ⑥ KMnO4和浓盐酸混合。
A.①②⑥ B.②④⑥ C.①③⑥ D.①④⑤⑥
(2)制取氯气时在烧瓶中加入一定量的MnO2,通过 (填仪器名称)向烧瓶中加入适量的浓盐酸,该反应的离子方程式: ;实验时为了除去氯气中的氯化氢气体,最好在A、B之间安装盛有 试剂的净化装置。
(3) 若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得Cl2的体积(标准状况下)
总是小于1.12 L的原因是
(4)①装置B中盛有 试剂(填序号)a.浓硫酸 b.碱石灰 c.五氧化二磷 d.无水氯化钙。其作用是
②装置C中的现象是 ;D中下层液体的现象是
③装置E中发生反应的离子方程式为
(5)乙同学认为甲同学的实验有缺陷,提出在 位置后(填字母)增加一个装置,该装置中应放入 试剂,其作用是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com