
题目列表(包括答案和解析)
A.方程式中x=4
B.达到平衡时,A、B两反应物的转化率之比为α(A):α(B)=3:1
C.若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,正逆反应的化学反应速率变小
D.在t℃时,若向原平衡混合物的容器中再充入amolC,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则应再充入a/4molB
| 1 |
| 27 |
| 1 |
| 27 |
 CH3CH2OH(g)+3H2O(g).
CH3CH2OH(g)+3H2O(g).| CO2转化率(%) n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
 CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______.
CH3OH(g)+H2O(g).2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L.下列判断不正确的是______.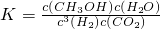 b.H2的平均反应速率为0.3mol/(L?s)
b.H2的平均反应速率为0.3mol/(L?s) 氧气”),b处电极上发生的电极反应是:______.
氧气”),b处电极上发生的电极反应是:______.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com